
题目列表(包括答案和解析)
23.(9分)现有0.1 mol某有机物A在8.96 L O2中充分燃烧后,气体体积变为6.72L,通过足量碱石灰吸收后剩余2.24 L(气体体积均在标准状况下测定)。
(1)燃烧后所得混合气体中CO2的物质的量为________,2.24 L剩余气体可能是________或________;
(2)若A是烃,其化学式可能是________________或________________;若A是烃的衍生物,其化学式可能是________________或________________。
(3)若A由丁醛(C4H8O)与气体B等物质的量混合得到,则气体B的化学式为________________或________________。
22.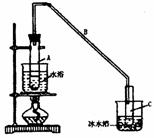 (11分)某化学小组采用类似制乙酸乙酯的装置(如右图),以环己醇制备环己烯,已知:
(11分)某化学小组采用类似制乙酸乙酯的装置(如右图),以环己醇制备环己烯,已知: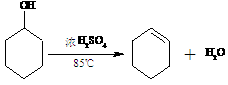
|
|
密度/g/cm3 |
熔点/℃ |
沸点/℃ |
溶解性 |
|
环己醇 |
0.96 |
25 |
161 |
能溶于水 |
|
环己烯 |
0.81 |
-103 |
83 |
难溶于水 |
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放人碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是________,导管B除了导气外还具有的作用是___________。
 ②试管C置于冰水浴中的目的是________。
②试管C置于冰水浴中的目的是________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加人饱和食盐水,振荡、静置、分层,环己烯在________层(填“上”或“下”),分液后用________(填入编号)洗涤。
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液
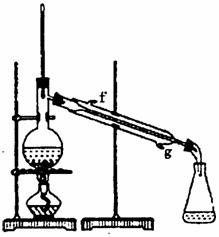
②再将环己烯按右图装置蒸馏,冷却水从________口进入。蒸馏时要加人生石灰,目的是________________________。
③收集产品时,控制的温度应在________℃左右。
(3)以下区分环己烯精品和粗品的方法,合理的是_______。
A.用酸性高锰酸钾溶液 B.用金属钠 C.测定沸点
21.(4分)某种混合物中可能含有甲酸、乙酸、甲醇及甲酸乙酯这些物质中的一k*s#5^u种或几种。在检验时有以下现象:
(1)有银镜反应;
(2)加入新制Cu(OH)2悬浊液,无变澄清的现象;
(3)与含碱的酚酞溶液共热,发现溶液中红色逐渐变浅以至无色。
根据上述现象,可以判断此混合物中一k*s#5^u定含有______________,可能含有______________,一k*s#5^u定没有______________。
20.(14分)A-J均为有机化合物,它们之间的转化如下图所示:
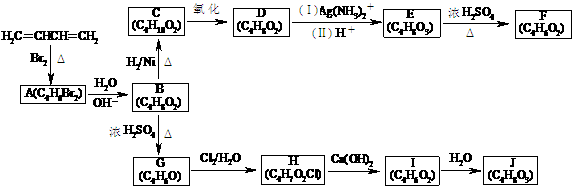
实验表明:
①D既能发生银镜反应,又能与金属钠反应放出氢气;
②核磁共振氢谱表明F分子中有三种氢,且其峰面积之比为1:1:1;
③G能使溴的四氯化碳溶液褪色;
④1 mol J与足量金属钠反应可放出22.4 L氢气(标准状况)。
请根据以上信息回答下列问题:
(1)A的结构简式为______________(不考虑立体结构),由A生成B的反应类型是_____反应;
(2)D的结构简式为________________________;
(3)由E生成F的化学方程式为________________,E中官能团有________________(填名称),与E具有相同官能团的E的同分异构体还有________________ (写出结构简式,不考虑立体结构);
(4)G的结构简式为________________;
(5)由I生成J的化学方程式________________。
19.(6分)由分子式及核磁共振氢谱写出该有机物的结构简式(图19-1)、(图19-2)
①C4H8 ②C10H14
强度比:1:3 强度比:5:9
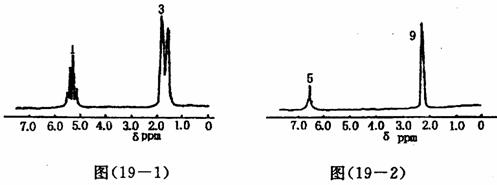
①结构简式:________________②结构简式:________________
18.(6分)完成下列反应方程式:
(1)苯乙烯与溴水反应__________________________________________;
(2)2-丁烯生成聚2-丁烯__________________________________________;
(3)苯与氯气在三氯化铁为催化剂时发生取代反应____________________________。
17.(4分)按要求完成下列填空
(1) 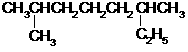 的系统命名是:____________________________。
的系统命名是:____________________________。
(2)3-甲基-2-戊烯的结构简式是____________________________。
22、(9分)0.2 mol某有机物在充有0.4 mol O2的密闭容器中燃烧,产物为由CO2、CO和H2O(g)组成的混合物。该混合物经过浓硫酸后,浓硫酸增重10.8 g,再通过灼热的CuO充分反应后,使CuO失重3.2 g,最后通过碱石灰,碱石灰增重17.6 g,若等量的该有机物能与9.2 g钠恰好完全反应。请通过计算,推断该有机物的分子式及结构简式。

21、(9分)根据甲酸分子的结构,预测甲酸可能具有的三种化学性质,并设计实验证实你的预测,简要写出实验方案。
化学性质① ,实验方案
化学性质② ,实验方案
化学性质③ ,实验方案
20、 (12分)
(12分)
根据图示回答下列问题:
(1)写出A、E、G的结构简式:A ,E ,G ;
(2)反应②的化学方程式(包括反应条件)是 ,
反应④化学方程式(包括反应条件)是 ;
(3)写出①、⑤的反应类型:① 、⑤ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com