
题目列表(包括答案和解析)
21、(8分)回答下列问题
(1)为减少大气污染,一些城市公共汽车逐步使用CNG清洁燃料,实验测得0.16g该气体燃料,完全燃烧生成224ml CO2(标准状况)和0.36g液态水,并放出8.903kJ的热量。请写出:CNG的化学式 ,其完全燃烧的热化学方程式
。
(2)拆开1mol H-H键,1mol N-H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则生成1molNH3的反应热△H= 。
(3)已知:H2O(g)=H2O(l) △H=-Q1KJ/mol
C2H5OH(g)=C2H5OH(l) △H=-Q2KJ/mol
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H=-Q3KJ/mol;则23g酒精液体完全燃烧的反应热(最后恢复到室温)△H= 。
20、(12分)(1)用惰性电极电解下列水溶液,请写出电极反应式及总反应式:
AgNO3: 阳极: 阴极:
总反应: 。
(2)普通班同学做:用Cu电极电解下列水溶液,请写出电极反应式及总反应式:
H2SO4:阳极: 阴极:
总反应: 。
(2)重点班同学做:科研人员新近开发出一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,可供手机连续使用一个月才充一次电,据此请回答以下问题:
①甲醇是________极,电极反应为___________________________。
②电池反应的离子方程式:__________________________________。
19、(7分)中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是_________________________。[
(2) 大烧杯上如不盖硬纸板,则求得的中和热数值_______(填“偏大”、“偏小’、“无影响”)
(3) 实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,
与上述实验相比,所放出的热量________(填“相等”或“不相等”),理由是____________
___________________________________;所求中和热的数值会________(填“相等”
或“不相等”),理由是__________________________________________________。
18、按如图甲装置进行实验,若乙中横坐标x表示流入电极的电子的物质的量,下列叙述不正确的是( )
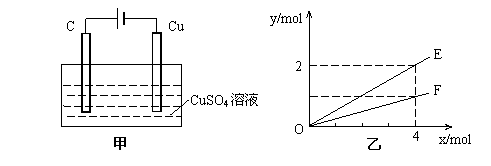

A.E表示生成铜的物质的量 B.E表示反应消耗水的物质的量
C.F表示反应生成氧气的物质的量 D.F表示生成硫酸的物质的量
17、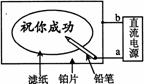 某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、
某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、
无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅
笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是( )
A 铅笔端作阳极,发生还原反应 B 铂片端作阴极,发生氧化反应
C 铅笔端有少量的氯气产生 D a点是负极,b点是正极
16、如右下图所示,A池用石墨电极电解NaOH溶液,B池精炼粗铜,一段时间后停止通电,A池中D极产生具有氧化性的气体在标准状况下为2.24L。下列说法正确的是( )
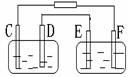 A.A池为电解池,B池为原电池
A.A池为电解池,B池为原电池
B.D、E两极都发生氧化反应
C.F极应与电源的负极相连
|
15、下列四种装置中,溶液的体积均为250 mL,开始时电解质溶液浓度均为0.10 mol·L-1,工作一段时间后,测得导线上均通过0.02 mole-,若不考虑溶液体积的变化,则下列叙述正确的是 ( )
A.工作一段时间后溶液的浓度①=②=③=④
B.工作一段时间后溶液的pH值:④>③>①>②
C.产生气体的总体积:④>③>①>②
D.电极上析出的固体的质量:①>②>③>④
14、甲、乙两个电解池均以Pt为电极,且互相串联,甲池盛有AgNO3溶液,乙池中盛有一定量的某盐溶液,通电一段时间后,测得甲池中某电极质量增加2.16 g,乙池中某电极上析出0.24 g金属,则乙池中溶质可能是( )
A.KNO3 B.MgSO4 C.CuSO4 D.Na2SO4
13、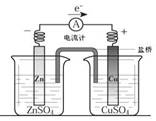 关于如右图所示装置的叙述,正确的是( )
关于如右图所示装置的叙述,正确的是( )
A.铜是阳极,铜片上有气泡产生
B.铜片质量逐渐减少
C.电流从锌片经导线流向铜片
D.铜离子在铜片表面被还原
12、下列关于铜电极的叙述,不正确的是( )
A.铜锌原电池中铜是正极 B.用电解法精炼粗铜时,粗铜作阳极
C.在镀件上电镀铜时可用金属铜作阳极 D.电解稀硫酸制H2、O2时,铜作阳极
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com