
题目列表(包括答案和解析)
5.下列说法不正确的是( )
A.能够发生化学反应的碰撞是有效碰撞
B.升高温度会加快化学反应速率,其原因是增加了活化分子的百分数
C.化学平衡发生移动,平衡常数必发生变化
D.测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸的起始温度、NaOH溶液的起始温度和反应后反应体系的最高温度
4.已知热化学方程式:SO2(g)+ O2(g)
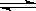 SO3(g) △H = ―98.32 kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
SO3(g) △H = ―98.32 kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
A. 196.64kJ B.196.64 kJ·mol-1 C.<196.64kJ D.>196.64kJ
3.本题所列的四个选项是4位同学在学习“化学反应速率和化学平衡”专题后,联系工业生产实际所发表的观点,你认为不正确的是( )
A.化学反应速率理论是研究怎样在一定时间内快出产品
B.化学平衡理论是研究怎样使用有限原料多出产品
C.化学反应速率理论是研究怎样提高原料转化率
D.化学平衡理论是研究怎样使原料尽可能多地转化为产品
2.下列有关电池的说法不正确的是( )
A.手机上用的锂离子电池属于二次电池
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
C.甲醇燃料电池可将化学能转化为电能
D.锌锰干电池中,锌电极是负极
1.下列叙述正确的是( )
A.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应 B.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” C.用电解水的方法制取大量氢气可以缓解能源不足的问题
D.升高温度活化能降低
14. 2.8g某单质A能从盐酸中置换出0.1g H2,同时生成ACl2;另一元素B,它的最高价 氧化物的化学式为BO3。在B的氢化物中,B的质量分数为94.1%。 计算A、B两种元素的相对原子质量。
13.X、Y、Z、W四种元素在元素周期表中原子序数逐渐增大。X为非金属元素,且X、W同主族,Y、Z为同周期的相邻元素。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。W原子的质子数等于Y、Z原子最外层电子数之和。试推断:
(1)Y的单质的电子式为 ,其中的化学键属于 键(填“离子”或“共价”)。
(2)X2Z的结构式为 ,空间构型 。
(3)写出有X、Y、Z所形成的共价化合物是 ;离子化合物是
此离子化合物与W的最高价氧化物对应水化物的溶液加热时反应的化学方程式是
;
12. A、B、C、D都是短周期元素,原子半径D>C>A>B。已知:A、B处于同一周期,A、C处于同一主族;C原子核内的质子数等于A、B原子核内的质子数之和;C原子最外层电子数是D原子最外层电子数的4倍。试回答:
(1)这四种元素分别是:A ,B ,C ,D ;
(2)这四种元素单质的熔点由高到低的顺序是(用化学式填写) ;
(3)C的单质是 晶体,B单质和C单质在常温下反应的生成物属于 晶体。
11. 在原子序数为1~18的元素中,其单质可以形成原子晶体的元素主要有 ,其单质是金属晶体的有 ,举出三种其单质是分子晶体且在常温下是气体的元素 。
10.下列物质的电子式书写正确的是 ( )
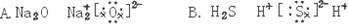
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com