
题目列表(包括答案和解析)
12.已知热化学方程式:SO2(g)+
O2(g)
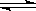 SO3(g) △H
= ―98.32 kJ/mol,在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为
SO3(g) △H
= ―98.32 kJ/mol,在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为
A. 196.64kJ B. 196.64kJ/mol
C. <196.64kJ D. >196.64kJ
11.硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
|
实验 |
反应温度/℃ |
Na2S2O3溶液 |
稀H2SO4 |
H2O |
||
|
V/mL |
c/mol·L-1 |
V/mL |
c/mol·L-1 |
V/mL |
||
|
A |
35 |
5 |
0.2 |
5 |
0.2 |
10 |
|
B |
25 |
5 |
0.2 |
5 |
0.2 |
10 |
|
C |
35 |
5 |
0.1 |
10 |
0.1 |
5 |
|
D |
25 |
5 |
0.1 |
10 |
0.1 |
5 |
10.汽车尾气无害化处理反应为2NO(g)+2CO(g) N2(g)+2CO2(g)。下列说法不正确的是
N2(g)+2CO2(g)。下列说法不正确的是
A.反应达到平衡后,NO的反应速率保持恒定
B.使用高效催化剂可有效提高该反应的正、逆反应速率
C.升高温度可使该反应的逆反应速率降低
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
9.反应A(g)+3B(g)  2C(g)在2L密闭容器中反应,半分钟内C的物质的量增加了0.6mol,有关反应速率中正确的是
2C(g)在2L密闭容器中反应,半分钟内C的物质的量增加了0.6mol,有关反应速率中正确的是
A.v(A)=0.005 mol·L-1·s-1 B.v(C)=0.02 mol·L-1·s-1
C.v(B)= v(A)/3 D..v(A)=0.01 mol·L-1·s-1
8. 在体积可变的容器中发生反应N2 + 3H2  NH3当增大压强使容器体积缩小时,化学反应速率加快,其主要原因是
NH3当增大压强使容器体积缩小时,化学反应速率加快,其主要原因是
A.分子运动速率加快,使反应物分子间的碰撞机会增多
B.反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
C.活化分子百分数未变,但单位体积内活化分子数增加,有效碰撞次数增多
D.分子间距离减小,使所有的活化分子间的碰撞都成为有效碰撞
7.对于在一定条件下进行的化学反应:2SO2+O2  2SO3,改变下列条件,可以提高反应物中的活化分子百分数的是
2SO3,改变下列条件,可以提高反应物中的活化分子百分数的是
A.升高温度 B.增大压强 C.压缩使容器体积变小 D.增大反应物浓度
6.下列有关电解精炼铜的说法中错误的是
A.粗铜做阴极
B.电解一段时间后,溶液中会存在锌、铁等不活泼的金属阳离子
C.阳极泥中含有金、银等贵重金属 D.电解质溶液可以选用硫酸铜溶液
5.有关铅蓄电池的说法中正确的是
A.该电池充电时的反应是一个自发反应
B.该电池放电过程发生的反应是一个自发反应
C.电池放电时,阳极发生还原反应
D.电池放电时,电解质溶液的PH下降
4.下列有关化学变化中的能量关系的说法中,错误的是
A.任何一个化学变化的过程中都包含着能量的变化
B. 化学变化过程中能量变化的实质就是旧键断裂要吸收能量,新键生成会放出能量
C.如果生成物的能量比反应物的能量高,则该反应为放热反应
D. 如不特别注明,化学反应的反应热就是就是该反应的焓变
3.下列有关锌锰干电池的说法中正确的是:
A.锌外壳是负极,石墨碳棒是正极材料
B. 在外电路中电子从碳棒流向锌外壳
C.电流从锌流到碳棒上
D. 在电池内部阳离子从碳棒向锌片移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com