
题目列表(包括答案和解析)
12.在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:
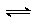 3A(g)+B(g) XC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB、3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都是0.2,下列叙述中正确的是
3A(g)+B(g) XC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB、3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都是0.2,下列叙述中正确的是
A.平衡时甲中A的体积分数为40%
B.平衡时,甲、乙两容器中A、B的物质的量之比不相等
C.若平衡时,甲、乙两容器中A的物质的量相等,则x=2
D.若平衡时,两容器中的压强不相等,则甲、乙两容器中压强之比为5:8
11.下列说法正确的是-s-5#u
A.0.03mol/L HA与0.03mol/L NaA等体积混合得到的碱性溶液中: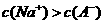
B.酸性溶液中水的电离程度一定比纯水的电离程度小
C.pH相等的CH3COONa、NaOH和Na2CO3三种溶液,
 k-s-5#u
k-s-5#u
D.室温下,pH=4的CH3COOH溶液和pH=10的NaOH溶液等体积混合后,pH大于7
10.已知:CH4(g)+2O2(g)→CO2(g)+2H2O(g) ΔH=-Q1 kJ/mol ;
2H2(g)+O2(g) == 2H2O(g) ΔH=- Q2 kJ/mol;
H2O(g) == H2O(l) ΔH=- Q3 kJ/mol
常温下,取体积比为4:1的甲烷和H2的混合气体112L(标准状况下),经完全燃烧后恢复到常温,则放出的热量为
A. 4Q1+0.5Q2 B. 4Q1+Q2+10Q3 C. 4Q1+2Q2 D. 4Q1+0.5Q2+9Q3
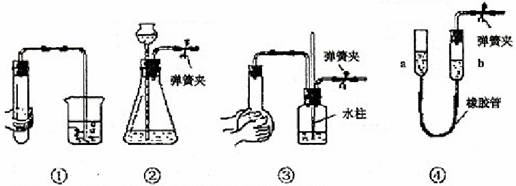
9.下列各装置中,夹紧②、③、④中的弹簧夹,并作相关操作,会漏气的装置是
 k-s-5#
k-s-5#
A.对装置①,双手移去后。导管中水面与烧杯水面相平
B.对装置②,长颈漏斗内液面高度保持不变
C.对装置③,长导管内形成一段水柱k-s-5#u
D.对装置④,上移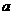 管后,
管后,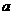 、
、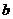 两端液面形成了一段稳定的高度差
两端液面形成了一段稳定的高度差
8.用铜片、银片、Cu (NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。以下有关该原电池的叙述正确的是
①在外电路中,电流由铜电极流向银电极 ②正极反应为:Ag++e-=Ag
③实验过程中取出盐桥,原电池仍可继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
A. ①② B.②③ C.②④ D.③④
7.在由水电离产生的H+浓度为1×10-13mol·L-1的溶液中,一定能大量共存的离子组是:① K+、Cl-、NO3-、S2- ② K+、Fe2+、I-、SO42- ③ Na+、Cl-、NO3-、SO42- ④Na+、Ca2+、Cl-、HCO3- ⑤ K+、Ba2+、Cl-、NO3-
A.②⑤ B.①③ C.③④ D.③⑤
6.A、B、C、D为四种短周期元素,已知A、C同主族,B、D同周期;A的气态氢化物比C的气态氢化物稳定;B的阳离子比D的阳离子氧化性强;B的阳离子比C的阴离子少一个电子层。下列叙述正确的是
A.原子序数:A>B>C>D B.单质熔点:D>B,A>C
C.原子半径:D>B>C>A D.简单离子半径:D>B>C>A
5.下列离子方程式正确的是
A.等物质的量的Ba(OH)2与明矾加入足量水中:
3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓
B.Fe(OH)3溶于氢碘酸: Fe(OH)3+3H+= Fe3++3H2O
C.向小苏打溶液中加入过量的石灰水:
Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O
D.氢氧化钠溶液中通入少量二氧化硫:SO2+OH-=HSO3-
4.NA代表阿伏加德罗常数,下列说法正确的是
A.标准状况下,2.24L溴乙烷中含有的溴离子数目为0.1×6.02×1023
B.25℃时,l L pH=13的Ba(OH)2 溶液中含有OH-的数目为0.1 NA
C.31g白磷中含有NA个共价键
D.标准状况下,2.24L NH3和CH4的混合气体,所含电子总数为2NA
3.将0.1mol·L-1CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起
A.溶液的pH增加 B.促进CH3COOH的电离
C.溶液的导电能力减弱 D.溶液中c(OH-)减少
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com