
题目列表(包括答案和解析)
5、有下列几种反应类型:① 消去 ② 加聚 ③ 水解 ④ 加成 ⑤ 还原 ⑥ 氧化,用丙醛制取1,2─丙二醇,按正确的合成路线依次发生的反应所属类型应是 ( )
A. ⑤①④③ B. ⑥④③① C. ①②③⑤ D. ⑤③④①
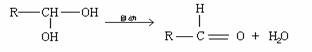
4、若1mol气态烃能跟2molHCl加成,而加成产物又可以和6molCl2完全取代,则该烃是( )
A.2-甲基丙烯 B.乙炔 C.1,3-丁二烯 D.丙炔
3、用18O标记的CH3CH218OH与乙酸反应制取乙酸乙酯,当反应达到平衡时,下列说法正确的是( )
A.18O只存在于乙酸乙酯中 B.18O存在于水、乙酸、乙醇以及乙酸乙酯中
C.18O存在于乙酸乙酯、乙醇中 D.若与丙酸反应生成的酯的相对分子质量为102
2、下列一卤代烷不能发生消去反应的是( )
A.CH3CH2Cl B. (CH3)2CHCl C. (CH3)3CCl D. (CH3)3CCH2Cl
1、新兴大脑营养学研究表明:大脑的发育与生长与不饱和脂肪酸有密切的关系,从深海鱼油中提取的被称作“脑黄金”的DHA就是一种不饱和程度很高的脂肪酸,它的分子中含6个碳碳双键,化学名称为:二十六碳六烯酸,它的分子组成应为( w.w.^w.k.&s.5* )
A .C25H50COOH B .C25H39COOH C .C26H41COOH D .C26H47COOH
26、某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定,完全反应时所得溶液pH大致为9 。下表是4种常见指示剂的变色范围:
|
指示剂 |
石蕊 |
甲基橙 |
甲基红 |
酚酞 |
|
变色范围(pH) |
5.0-8.0 |
3.1-4.4 |
4.4-6.2 |
8.2-10.0 |
 (1)该实验应选用
作指示剂,向锥形瓶中移取一定体积的白醋所用的滴定管是
。( 酸式滴定管 或 碱式滴定管 )
(1)该实验应选用
作指示剂,向锥形瓶中移取一定体积的白醋所用的滴定管是
。( 酸式滴定管 或 碱式滴定管 )
(2)右图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为 mL,设此时液体体积读数为 a ml ,滴定管中液体的体积 V (=、>、<) ( 50-a ) ml
(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下:
|
实验次数 |
第一次 |
第二次 |
第三次 |
|
消耗NaOH溶液体积/mL |
26.02 |
25.35 |
25.30 |
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是 (4分)
A.实验结束时俯视刻度线读取滴定终点时NaOH溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):
C= mol/L。k*s*5*u
25、今有①CH3COOH;②HCl;③H2SO4三种溶液,选择填空:
A.①>②>③ B.①<②<③ C.①=②=③ E.①>②=③
D.①=③>② F.①<②=③ G.①=②<③ H.①=②>③
(1)当它们pH相同时,其物质的量浓度关系是 。k*s*5*u
(2)当它们pH相同、体积相同时,同时加入锌,则开始时反应速率大小关系为 。
(3)中和等体积、等物质的量浓度的三种酸溶液,需同物质的量浓度的烧碱溶液的体积关系为 。
(4)将pH相同的三种酸均稀释10倍后,pH关系为
24、在稀氨水中存在下述电离平衡NH3+H2O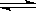 NH3 ·H2O
NH3 ·H2O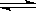 NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”“减小”或“不变”);平衡移动方向如何?(填“正反应方向”逆反应方向”或“不变”)
NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”“减小”或“不变”);平衡移动方向如何?(填“正反应方向”逆反应方向”或“不变”)
|
加入的物质 |
少量(NH4)2SO4固体 |
少量HNO3溶液 |
少量KOH溶液 |
|
c(OH-)的变化 |
|
|
|
|
平衡移动方向 |
|
|
|
23、(1)在一定条件下的下列可逆反应达到平衡时,试填出:xA+yB zC
zC
1 若A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z关系是
___________ _____;
2 若C是气体,并且x+y=z,在加压时化学平衡可发生移动,则平衡必定是向___ __方向移动(填“正”或“逆”);
3 已知B、C是气体,现增加A物质的量,平衡不移动,说明A是 (填状态);
4 如加热后,C的百分含量减小,则正反应是________热反应。
 (2)右图表示在密闭容器中反应:
(2)右图表示在密闭容器中反应:
2SO2(g)+O2(g)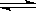 2SO3(g),⊿H<0;达到平衡时,
2SO3(g),⊿H<0;达到平衡时,
由于条件改变而引起反应速率和化学平衡的变化情况,
1a时刻改变的条件可能是 ;
2b时刻改变的条件可能是 ;
3若C时刻增大压强,反应速率变化情况画在c~d处.
22、选择适宜的材料和试剂设计一个原电池,完成下列反应:
Zn + CuSO4 = ZnSO4 + Cu[
(1)在右边方框内画出装置图,并标明各部分材料名称
(2)负极材料 ,
电解质溶液是 。
(3)写出电极反应式:
正极: ;
负极: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com