
题目列表(包括答案和解析)
9.实验室用足量的锌与稀硫酸反应制备氢气。为减慢反应速率,又不影响生成氢气的总量,可采用下列哪种方法
A.加入CH3COONa固体 B.加入KNO3固体
C.加入NaOH固体 D.加入几滴硫酸铜溶液
8.可促进HClO的电离,并使溶液pH增大的是
①加入HCl;②加入NaClO;③加入NaOH;④加入Zn;⑤加热
A.①②③④ B.②③④ C.③④ D.③④⑤
7.用湿玻璃棒蘸取某溶液测定其pH,其测定结果
A.偏高 B.偏低
C.无影响 D.无法判断
6.下列事实一定能说明HNO2是弱电解质的是
①常温下,NaNO2溶液的pH大于7;②用HNO2溶液做导电性实验,灯泡很暗;③0.1mol/L的HNO2溶液的pH为2.1;④常温下,将pH=3的HNO2稀释100倍后,pH<5
A.①②③ B.②③④ C.①③④ D.②④
5.为了避免溶液中CuSO4因水解发生沉淀,正确的操作方法是
A.稀释 B.加稀硫酸 C.加NaOH溶液 D.加热
4.下列各电离方程式中书写正确的是
A.CH3COOH=H++CH3COO- B.CO32-+2H2O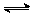 H2CO3+2OH-
H2CO3+2OH-
C.Al(OH)3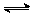 Al3++3OH- D.NaH2PO4
Al3++3OH- D.NaH2PO4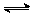 Na++H2PO4-
Na++H2PO4-
3.在一密闭容器中充入一定量的N2和H2,N2(g)+3H2(g)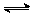 2NH3(g),经测定反应开始后的2s内氢气的平均速率υ(H2)=0.45mol/(L·s),则2s末NH3的浓度为
2NH3(g),经测定反应开始后的2s内氢气的平均速率υ(H2)=0.45mol/(L·s),则2s末NH3的浓度为
A.0.30mol/L B.0.60mol/L C.0.45mol/L D.0.55mol/L
2.下列微粒对水的电离平衡不产生影响的是
A.H3O+ B.OH- C.NH4+ D.NO3-
1.下列各组物质中,前者为强电解质,后者为弱电解质的是
A.硫酸,硫酸镁 B.碳酸,碳酸钠
C.食盐,酒精 D.碳酸氢钠,醋酸
23.某学生用0.1 mol/L的KOH标准溶液滴定未知浓度盐酸,其操作分解为如下几步:
A.移取20 mL待测盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
B.用标准溶液润洗滴定管2-3次
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至0刻度以上2-3 cm
E.调节液面至0或0以下刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度。
就此实验完成填空
(1)正确操作步骤的顺序是(用序号字母填写)____________________________;
(2)上述B步骤操作的目的是________________________________________________;
(3)上述A步骤操作之前,先用待测液润洗锥形瓶,则对滴定结果的影响是________;
(4)判断到达滴定终点的实验现象是_____________________________________;
(5)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸则对滴定结果产生的影响是____________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com