
题目列表(包括答案和解析)
6.一个电子排布为1s22s22p63s23p1的元素最可能的价态是
A. +1 B. +2 C. +3 D. -1
5.下列元素的电负性最大的是
A.Na B.S C.O D.C
4.根据电子排布的特点,Cu在周期表中属于
A.s区 B.p区 C.d 区 D.ds区
3.下列能层中,有f能级的是
A.K B.L C.M D.N
2.仔细观察下列图形,则它表示的是晶体还是非晶体
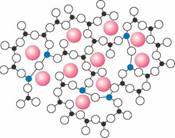
A.是晶体 B.可能是晶体,可能是非晶体
C.是非晶体 D.不能确定
1. 下列关于电子云的说法中,正确的是
下列关于电子云的说法中,正确的是
A.电子云表示电子在原子核外运动的轨迹
B.电子云表示电子在核外单位体积的空间出现机会的多少
C.电子云界面图中的小黑点密表示该核外空间的电子多
D.电子云可表示电子在核外运动的方向
14. 下列化学实验事实及其解释都正确的是
A.向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘
B.向SO2水溶液中滴加盐酸酸化的BaCl2溶液,有白色沉淀生成,说明BaSO3难溶于盐酸
C.向0.1 mol·L-1FeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色,说明Fe2+具有氧化性
D.向2.0 mL浓度均为0.1 mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01 mol·L-1AgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp大
特别提醒:请将选择题答案填写在答题纸的表格中!
洪泽中学2009-2010学年度高二年级第二学期期中考试
13. 已知复分解反应2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑可自发进行。在常温下, 测得浓度均为0.1mol·L-1的下列六种溶液的pH:
|
溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
|
pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
表中数据揭示出复分解反应的一条规律,即碱性较强的物质发生类似反应可以生成碱性 弱的物质。依照该规律,请你判断下列反应不能成立的是
A.CO2+H2O+2NaClO=Na2CO3+2HClO
B.CO2+H2O+NaClO=NaHCO3+HClO
C.CH3COOH+NaCN=CH3COONa+HCN
D.CO2+H2O+2C6H5ONa→Na2CO3+2C6H5OH
12.可逆反应aA(g)+bB(s) cC(g)+dD(g)在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是
cC(g)+dD(g)在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是
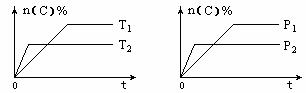
A.温度降低,化学平衡向逆反应方向移动
B.使用催化剂,C的物质的量分数增加
C.化学方程式系数a<c+d
D.无法根据图像确定改变温度后化学平衡移动方向
11. 室温下,某溶液中由水电离的c(OH-)为1.0×10-12 mol·L-1,下列离子在该溶液中一定能大量共存的是
A.NH4+、Na+ 、SO42- 、Cl- B.Ba2+、 K+ 、ClO-、NO3-
C.Ba2+、 K+ 、Cl-、NO3- D.Na+ 、Ca2+ 、Cl- 、AlO2-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com