
题目列表(包括答案和解析)
6.pH相同的盐酸和醋酸两种溶液中,它们的
A.H+的物质的量相同 B.物质的量浓度相同
C.H+的物质的量浓度不同 D.H+的物质的量浓度相同
5. 在温度不变的条件下,体积恒定不变的密闭容器中发生如下反应:2SO2+O2 2SO3,下列叙述能够说明反应已经达到平衡状态的是
2SO3,下列叙述能够说明反应已经达到平衡状态的是
A.容器中SO2、O2、SO3共存
B.反应容器中压强不随时间变化
C.容器中SO2、O2、SO3的物质的量之比为2∶1∶2
D. SO2与SO3的浓度相等
4. 在一密闭容器内发生氨分解反应2NH3 N2+3H2。已知NH3起始浓度是2.6 mol·L-1,4s末为1.0 mol·L-1,若用NH3的浓度变化来表示此反应的速率,则v(NH3)应为
N2+3H2。已知NH3起始浓度是2.6 mol·L-1,4s末为1.0 mol·L-1,若用NH3的浓度变化来表示此反应的速率,则v(NH3)应为
A.1.6 mol·L-1·s-1 B.0.8 mol·L-1·s-1
C.0.4 mol·L-1 ·s-1 D. 0.04 mol·L-1·s-1
3. 设反应C+CO2  2CO(正反应吸热)反应速率为v1,N2+3H2
2CO(正反应吸热)反应速率为v1,N2+3H2  2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1、v2的变化情况为
2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1、v2的变化情况为
A.同时增大 B.同时减小
C.v1增大,v2减小 D. v1减小,v2增大
2.下列各组热化学方程式中,化学反应的△H前者大于后者的是
①C(s)+O2(g)===CO2(g);△H1 C(s)+O2(g)===CO(g);△H2
②S(s)+O2(g)===SO2(g);△H3 S(g)+O2(g)===SO2(g);△H4
③H2(g)+O2(g)===H2O(l);△H5 2H2(g)+O2(g)===2H2O(l);△H6
④CaCO3(s)===CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)===Ca(OH)2(s);△H8
A.① B.④ C.②③④ D.①②③
1.下列说法正确的是
A.热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量。
B.热化学方程式中,如果没有注明温度和压强,则表示在标准状况下测得的数据。
C.书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态。
D.凡是化合反应都是放热反应,分解反应都是吸热反应。
27. (1)甲、乙两种元素是同一周期的相邻元素,甲元素是形成有机物的主要元素,乙元素的p亚层上有3个电子。
写出甲元素原子的核外电子排布式 。下列各化合物分子中甲元素的原子轨道杂化方式全部相同的是 (填序号)。
a.CH2=CH-C≡CH b.CH2=C(CH3)一CH=CH2 C.C(CH2OH)4
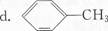
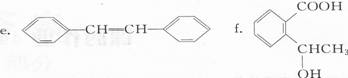
(2)下列现象和应用与电子跃迁无关的是( ).
A.激光 B.焰色反应 C.燃烧放热 D.原子光谱 E.霓虹灯 F.石墨导电
(3)A、B、C三种短周期元素,A是原子半径最小的元素,B原子最外层电子数是次外层的两倍,C元素的基态原子L层有两个未成对电子.
①某直线形分子由A、B两种元素组成且原子个数比为l:1,该分子中含有 个σ键, 个∏键.
②由A、B、C三种元素组成的无机阴离子,可形成二聚离子或多聚链状离子,从该阴离子的结构特点分析能够相互缔合的原因:
(4)CO的结构式可表示为C≡0.N2的结构式可表示为N≡N.下表是两者的键能数据:(单位:kJ·mol_。)
|
|
A-B |
A=B |
A≡B |
|
C≡0 |
357.7 |
798.9 |
1071.9 |
|
N≡N |
154.8 |
418.4 |
941.7 |
结合数据说明CO比N2活泼的原因:
(5)Fe、Co、Ni、Cu等金属能形成配合物与这些金属原子的电子层结构有关.
①Fe(CO)5常温下呈液态.熔点为一20.5℃.沸点为 103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于 (填晶体类型).
②CuSO5·5H20(胆矾)中含有水合铜离子因而呈蓝色.写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)
26.已知和碳元素同主族的X元素位于周期表中的第1个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们所形成化合物的分子式是XY4。试回答:
(1)X元素的原子基态时电子排布式为 ;Y元素原子最外层电子的电子排布图为 。
(2)该化合物的空间结构为 ,中心原子的杂化类型为 ,
(3)该化合物在常温下为液体,该化合物中分子间作用力是 。
(4)该化合物的沸点与SiCl4比较, (填化学式)的高,原因是 .
25.Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物,其固态属于 晶体,俗名叫 ;
(2)R的氢化物分子的空间构型是 ,属于 分子(填“极性”或“非极性”);它与X 形成的化合物可作为一种重要的陶瓷材料,其化学式是 ;
(3)X的常见氢化物的空间构型是 ;它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是 ;
(4)Q分别与Y、Z形成的共价化合物的化学式是 和 ;Q与Y形成的分子的电子式是 ,属于 分子(填“极性”或“非极性”)。
24. X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:
①X元素原子价电子排布为nS2np2,且原子半径是同族元素中最小的。
②Y元素是地壳中含量最多的元素;w元素的电负性略小于Y元素,在w原子的电子排布中,p轨道上只有1个未成对电子。
③Z元素的电离能数据见下表(kJ·mol_):
|
Ⅰ1 |
Ⅰ2 |
Ⅰ3 |
Ⅰ4 |
… |
|
496 |
4562 |
6912 |
9540 |
… |
请回答:
(1)Z2Y2的电子式为 ,含有的化学键类型为 ,Z2Y2为 晶体。
(2)X、Y、Z三种元素所形成的常见化合物的名称为 ;XY2的结构式为 ,分子空间构型为
 (3)X、Y、Z、W四种元素所形成的单质中,熔点最高、硬度最大的是
(填“名称”);晶体ZW的熔点比晶体XW4明显高的原因是
。
(3)X、Y、Z、W四种元素所形成的单质中,熔点最高、硬度最大的是
(填“名称”);晶体ZW的熔点比晶体XW4明显高的原因是
。
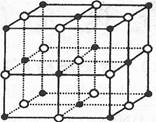
(4)ZW晶体的结构示意图如下。已知ρ(ZW)=2.2 g·cm 一3,NA=6.02×1023 mol-,则ZW晶体中两个最近的Z离子中心间的距离为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com