
题目列表(包括答案和解析)
36.(4分)有A、B、C、D 四种溶液,其中阳离子分别为Ag+、Ba2+、Al3+、Fe3+,阴离子分别为Cl-、NO3-、OH-、SO42-。四种溶液中阴、阳离子都不重复。现进行如下实验:
①C溶液中加入铁粉,溶液质量增加;
②在A溶液中滴入酚酞试液,溶液呈红色;
③在B溶液中逐滴滴入过量氨水时,先出现沉淀,后沉淀逐渐消失;
④在B和D溶液中分别加入硝酸钡溶液,均无明显现象。
由上述现象可推知各种溶液中溶质的化学式分别是:
A___________,B___________,C___________,D___________。
35.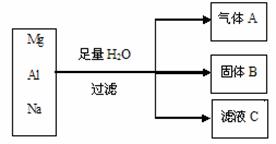 (5分)现有Na、Mg及Al组成的混合物,往其中加入足量水后,变化关系如下图所示。填写以下空格。
(5分)现有Na、Mg及Al组成的混合物,往其中加入足量水后,变化关系如下图所示。填写以下空格。
(1)气体A是 。
(2)固体B中一定含有的一种金属是 ,可能含有的金属是 。
(3)溶液C中一定含有的阴离子是 ,阳离子是 (注:不考虑水的电离)。
34.(8分)某化学课外活动小组,从化学手册上查得硫酸铜在500 ℃以上按下式分解:CuSO4 CuO+SO2↑+SO3↑+O2↑,便决定设计一验证性实验探索测定反应产生的SO2、SO3和O2的物质的量,并经计算以此确定该条件下CuSO4分解反应方程式中各物质的化学计量数。实验可能用到的仪器如下图所示:
CuO+SO2↑+SO3↑+O2↑,便决定设计一验证性实验探索测定反应产生的SO2、SO3和O2的物质的量,并经计算以此确定该条件下CuSO4分解反应方程式中各物质的化学计量数。实验可能用到的仪器如下图所示:
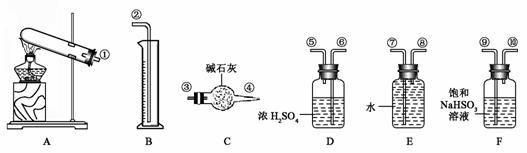
实验测得数据及有关结果如下:
①准确称取6.0 g无水CuSO4 ;②干燥管总质量在实验结束时增加了2.4 g ;③测出量筒中水的体积后,折算成排水的气体,在标准状况下的体积为280 mL;④实验结束时,装置F中的溶液变为NaHSO4溶液(不含其他杂质)。
试回答下列问题:
(1)按装置从左至右的方向,各仪器接口连接顺序为____________ _________(填数字序号)。
(2)装置F的作用是__________________________ ___________________。
(3)装置D的作用是________________________ _____________________。
(4) 通过计算,推断出该条件下反应的化学方程式:_________ _________________。
33.(8分)已知:“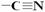 ”(氰基)在酸性条件水解可以生成“-COOH”。
”(氰基)在酸性条件水解可以生成“-COOH”。

|
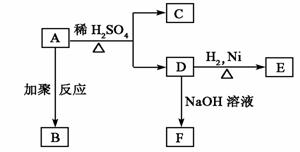 将A涂在手术后伤口的表面,在数秒内A迅速固化并起粘结作用,以代替通常的缝合。在适宜条件下A可以发生如下一系列转化:
将A涂在手术后伤口的表面,在数秒内A迅速固化并起粘结作用,以代替通常的缝合。在适宜条件下A可以发生如下一系列转化:
请回答下列问题:
(1)D分子结构中含有的官能团的名称是 。
(2)D转化为E的反应属于(选填序号) 。
A.取代反应 B.加成反应 C.氧化反应 D.还原反应
(3)由A生成B的化学反应方程式是:
(4)E有多种同分异构体,在这些物质中,与E属于同系物的有机物有________ 种(除E外)。
(5)若1 mol D和含足量的NaHCO3的溶液充分混合,完全反应,则所生成标准状况下气体体积为 L。
32.(5分)右图为A、B、C三种短周期元素在周期表的相对位置,且三种元素的原子序数之和为31,又知A元素的单质在空气中含量最高。回答下列问题:
(1) A元素的名称为 ,C元素的一种氧化物排放到大气中,是导致形成酸雨的主要物质,该氧化物的化学式为 。
(2)B元素的某种氢化物通常用于做溶剂,此氢化物的电子式是 ,C元素的阴离子结构示意图是 ,三种元素的原子半径中最小的是 (填元素符号)。
31.(6分)
(1)写出铁与水蒸气反应的化学方程式
(2)写出碳酸钠水解的离子方程式
(3)写出实验室加热酒精和浓硫酸的混合液制乙烯的化学方程式 ,反应类型 。
(4)苯酚与溴水反应的化学方程式 ,反应类型 。
|
A |
B |
|
|
C |
30.在FeCl3、CuCl2、FeCl2的混合溶液中,Fe3+、Cu2+、Fe2+的物质的量浓度之比为4︰2︰1,现加入适量的铁粉,使溶液中的三种离子的物质的量浓度之比为1︰3︰9,则投入的铁粉与原溶液中Cu2+的物质的量之比为( )
A 5︰4 B 4︰5 C 3︰5 D 5︰6
卷Ⅱ(共40分)
29.下列物质中,加入FeCl3溶液显紫色的是( )
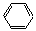

A. -CH2OH B. -OH
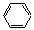
C. C2H5-OH D. -Cl
28.将 ① H+ ②Cl- ③Al3+ ④K+ ⑤F- 五种粒子分别加入水中,基本上不影响水的电离
平衡的有( )
A.①③⑤ B.②④ C.②④⑤ D.①②④⑤
27.下列反应的离子方程式不正确的是( )
A.向烧碱溶液中滴加少量氯化铝溶液 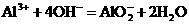
B.物质的量相等的溴化亚铁跟氯气反应
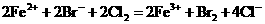
C.硫化钾晶体溶于水 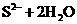


D.向碳酸钠溶液中滴加过量的稀硫酸 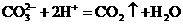
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com