
题目列表(包括答案和解析)
26.(13分)(1)为体现绿色世博、低碳世博、科技世博,上海世博会已经开始使用中国自己生产的燃料电池汽车,该车以氢气和空气中的氧气为燃料,KOH为电解质溶液,真正实现了“零排放”。该电池的负极反应式为 ,从能量角度分析氢气用作燃料电池与直接燃烧相比主要优点是 。
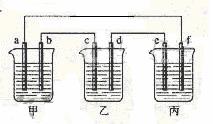 (2)下图所示装置中,a、b、e、f电极为石墨,c、d电极分别为Cu和Zn,甲中为200ml 3mol/LNaCl溶液,乙中为200ml2mol/LH2SO4,丙中为200mlCuSO4和K2SO4混合溶液。
(2)下图所示装置中,a、b、e、f电极为石墨,c、d电极分别为Cu和Zn,甲中为200ml 3mol/LNaCl溶液,乙中为200ml2mol/LH2SO4,丙中为200mlCuSO4和K2SO4混合溶液。
①从能量转化的角度,乙是 装置,
阳离子移向 极(填c或d)
②检验b电极产物的方法是 ,甲池子中总反应方程式为 ,忽略溶液体积变化,当d电极质量变化6.5g时,甲池中溶液的PH=
③已知丙池中c(SO42-)=2mol/L。工作一段时间后,两极分别产生标况下的气体各2.24L,则原混合溶液中c(K+)是 。
25.已知某溶液中只存在OH-、H+、Cl-、NH4+四种离子,其离子浓度可能有如下关系:
① c(Cl-)>c(NH4+)>c(H+)>c(OH-)
② c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③ c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④ c(NH4+) =c(Cl-)>c(OH-)=c(H+)
下列说法正确的是
A.若①正确,则溶液中溶质一定为NH4Cl
B.若③正确,则溶液中c(NH3·H2O) + c(NH4+)>c(Cl-)
C.若④正确,且盐酸和氨水体积相等,则盐酸中c(H+)等于氨水中c(OH-)
D.溶质不同时,上述四种关系式均可能成立
24、下列四种装置中,溶液的体积均为250mL,开始时电解质溶液的浓度均为0.10mol/L,工作一段时间后,测得导线上均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述正确的是
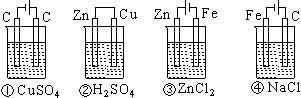
A 工作一段时间后原溶质的浓度①=②=③=④
B 工作一段时间后溶液的pH值:④>③>①>②
C 产生气体的总体积:④>③>①>②
D 电极上析出的固体的质量:①>②>③>④
22、某同学按右图所示的装置进行电解实验。下列说法正确
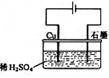 A.电解过程中,铜电极上有H2产生
A.电解过程中,铜电极上有H2产生
B.电解初期,主反应方程式为:Cu+H2SO4 CuSO4+H2↑
CuSO4+H2↑
C.电解一定时间后,石墨电极上有铜析出
D.整个电解过程中,H+的浓度不断增大
23 已知25℃时有关弱酸的电离平衡常数:
|
弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
|
电离平衡常数(25℃) |
1.8×l0-5 |
4.9×l0-10 |
K1=4.3×l0-7 K2=5.6×l0-11 |
则下列有关说法正确的是( )
A、等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B、a mol·L-1 HCN溶液与b mol·L-1 NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b
C、冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离程度、pH均先增大后减小
D、NaHCO3和Na2CO3等物质的量混合溶液中,一定存在:
c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
21. 铅蓄电池是最重要的二次电池,其正极板上覆盖有PbO2,负极板上覆盖有Pb,电解质是硫酸溶液,下列说法不正确的是
A.充电时转移1mol电子则生成0.5mol H2SO4
B.放电时正极的电极反应为:PbO2 + 4H+ + SO42- + 2e- = PbSO4 + 2H2O
C.充电时,电池上标注“+”的电极应与外接电源的正极相连
D.放电时,Pb失电子发生氧化反应
20、下列说法正确的是( )
A.在一定温度下AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数;
B.AgCl的Ksp=1.8×10-10 mol2·L-2,在任何含AgCl固体的溶液中,c(Ag+)=c(Cl-)且Ag+与Cl-浓度的乘积等于1.8×10-10 mol2·L-2;
C.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液;
D.向饱和AgCl水溶液中加入盐酸,Ksp值变大。
19.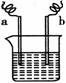 右图中,两电极上发生电极反应。a极:Cu2++2e-=Cu,b极:Fe-2e-==Fe2+下列说法不正确的是( )
右图中,两电极上发生电极反应。a极:Cu2++2e-=Cu,b极:Fe-2e-==Fe2+下列说法不正确的是( )
A.装置中电解质溶液一定含有Cu2+
B.该装置一定是化学能转化为电能
C.a极上一定发生还原反应
D.a、b可能是同种电极材料
18. 为了使Na2S溶液中c(Na+)/ c(S2-)的比值变小,可加入的物质是
A. 适量盐酸 B. 适量NaOH溶液 C. 适量KOH溶液 D. 适量KHS溶液
17.某温度下,重水D2O的离子积为1.6×10-15,若用pH一样的定义来规定
pD=-lgc(D+),以下关于pD的叙述正确的是 ( )
A.中性溶液的pD=7.0.
B.含0.01 mol的NaOD的D2O溶液1L,其pD=12.0.
C.溶解0.01 mol的DCl的D2O溶液1L,其pD=2.0.
D.在100 mL 0.25 mol·L-1的DCl重水溶液中,加入50 mL 0.2mol·L-1的NaOD的
重水溶液,其pD=1.0.
16.化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂,
HIn(aq) H+(aq)+In-(aq)
H+(aq)+In-(aq)
红色 黄色
将下列物质加入到HIn水溶液中,最终可使溶液显黄色的是
A.HCl B.SO3 C.NH3·H2O D.Na2O2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com