
题目列表(包括答案和解析)
25、(8分)现有常见有机物A,在压强为1.01×105Pa 、120OC时,取A气体20毫升,与相同状况下x毫升氧气混合。
(1) 如果A为烃,完全燃烧恢复到原状况后体积增至x+40毫升,那么A在组成上应满足的条件是
(2) 如果A为两种有机物组成的混合物,当x=25毫升是恰好完全燃烧,恢复到原状况后,测得生成二氧化碳和水的总体积为50毫升,平均相对分子质量为28.4.试回答
① 生成二氧化碳和水的体积比为
② A的可能组成是
河北冀州中学2009-20010学年下学期期中
24、(11分)请根据下图回答:
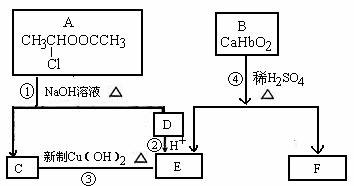
已知:一个碳原子上连有两个羟基时,易发生下列转化:
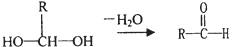
(1)E中含有的官能团的名称是 。
(2)反应③的化学方程式是 。
(3)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2): n(H2O)=2:1,则B的分子式为 。
(4)F是高分子光阻剂生产的主要原料。F具有如下特点:
①能跟FeCl3溶液发生显色反应; ②能发生加聚反应;③苯环上的一氯代物只有两种。
F在一定条件下发生加聚反应的化学方程式为 。
(5)化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。写出G所有可能的结构式
23、(16分)Fe(OH)2中一种白色沉淀,在空气中或在含有O2的水中容易被氧化而变色,难以看到它的“真面目”。为了解决这个问题,许多科学家对此实验作了研究和改进,以下三个图有一定的代表性。
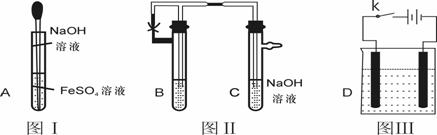
(1)按照常规实验的要求,用胶头滴管滴加溶液时 (填“能”或“不能”)伸入试管中,原因是 ,图I中,长胶头滴管伸入液面下的目的是 ;
(2)在图Ⅱ中,要观察到Fe(OH)2的生成,B管中的试剂可以是 C中氢氧化钠溶液应预先处理的方法是 在反应试剂加入后的实验操作步骤是
①打开止水夹并
②
若操作步骤①和②颠倒,能否看到Fe(OH)2白色沉淀? 理由是:
(3)若用图Ⅲ装置实验制备Fe(OH)2,阳极材料应选用 ,阴极用石墨,阳极反应是 ,阴极反应是 ,若在电极上生成白色沉淀,则电解质溶液应选用____ ;(填序号)若在两极之间的溶液中生成白色沉淀,则电解质溶液是___ ____.(填序号)
a.纯水 b.NaCl 溶液 c.NaOH溶液 d.CuCl2溶液
若能长久看到Fe(OH)2白色沉淀的生成,该实验的明显不足是 ,
改进措施是 。
22、(9分)现有五种离子化合物A、B、C、D和E,都是由下表中离子形成的:
|
阳离子 |
Ag+
Ba2+ A1+ |
|
阴离子 |
OH-
C1- SO42- |
为鉴别它们,分别完成以下实验,其结果是: a.B和D都不溶于水,也不溶于酸; b.A溶于水后,与上述某阳离子反应可生成B,且A溶液与过量氨水反应生成白色沉淀; c.C溶于水后,与上述某阳离子反应可生成D,且C溶液与过量氨水反应生成白色沉淀。 d.E溶于水后,与上述某阴离子反应可生成B; e.A溶液与适量E溶液反应生成沉淀,再加入过量E溶液,沉淀量减少,但不消失。 请根据上述实验结果,填空: (1)写出下列化合物的化学式:A B , C ,D E
(2)写出C与氨水反应的离子方程式
(3)A溶液与过量的E溶液反应的离子方程式 。
21、填空(16分)
(1)已知氯化铝的熔点为190OC(2.02×105Pa),但它在180OC即开始升华. 在500K和1.01×105Pa时,它的蒸气密度(换算成标准状况时)为11.92g/L,氯化铝属于______ _晶体.是 化合物 在500K和1.01×105Pa时,其化学式为 ,无水氯化铝在潮湿空气中强烈地“发烟”,其原因是_________.(用化学方程式表示)
(2)已知充分燃烧a g乙炔气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式的是
(3)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
NO3-+4H++3e- →NO+2H2O
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
①写出并配平该氧化还原反应的方程式:
②反应中硝酸体现了 、 性质。
③反应中若产生0.2mol气体,则转移电子的物质的量是 mol。
④若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是: 。
20、某有机化合物仅由碳、氢、氧三种元素组成,其相对分子质量小于150,若已知其中氧的质量分数为 50%,则分子中碳原子的个数最多为 ( )
A.4 B.5 C.6 D.7
非选择题(共60分)
19、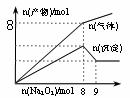 将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热, 产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如图所示。则原溶液中Al3+、Mg2+、NH4+的物质的量分别为( )
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热, 产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如图所示。则原溶液中Al3+、Mg2+、NH4+的物质的量分别为( )
A.2 mol、3 mol、8 mol B.3 mol、2 mol、8 mol
C.2 mol、3 mol、4 mol D.3 mol、2 mol、4 mol
18、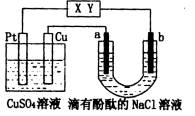 .如图所示,a、b是石墨电极,通电一段时间后,b极附
近溶液显红色。下列说法正确的是
A.X极是电源负极,Y极是电源正极
B.Pt极上有6.4gCu析出时,b极产生2.24L(标准状况)气体
C.电解过程中 CuSO4溶液的pH逐渐增大
D.a极的电极反应式为:2C1--2e-=C12↑
.如图所示,a、b是石墨电极,通电一段时间后,b极附
近溶液显红色。下列说法正确的是
A.X极是电源负极,Y极是电源正极
B.Pt极上有6.4gCu析出时,b极产生2.24L(标准状况)气体
C.电解过程中 CuSO4溶液的pH逐渐增大
D.a极的电极反应式为:2C1--2e-=C12↑
17、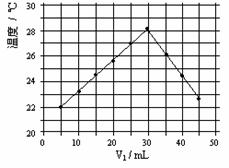 将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH 溶液混合均匀后测量并记录溶液温度,实验结果如右图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是
A、做该实验时环境温度为22℃
B、该实验表明化学能可能转化为热能
将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH 溶液混合均匀后测量并记录溶液温度,实验结果如右图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是
A、做该实验时环境温度为22℃
B、该实验表明化学能可能转化为热能
C、NaOH溶液的浓度约为1.0mol/L D、该实验表明有水生成的反应都是放热反应
16、将用于2008年北京奥运会的国家游泳中心(水立方)的建筑采用了膜材料ETFE,该材料为四氟乙烯与乙烯的共聚物,四氟乙烯也可与六氟丙烯共聚成全氟乙丙烯。下列说法错误的是
A.ETFE分子中可能存在“-CH2-CH2-CF2-CF2-”的连接方式
B.合成ETFE及合成聚全氟乙丙烯的反应均为加聚反应
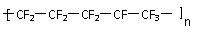 C.聚全氟乙丙烯分子的结构简式可能为
C.聚全氟乙丙烯分子的结构简式可能为
D.四氟乙烯中既含有极性键又含有非极性键
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com