
题目列表(包括答案和解析)
14、某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。
下列说法正确的是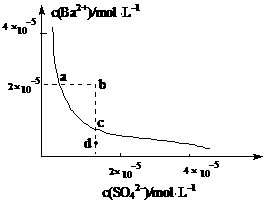
A.加入Na2 SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
13、用石墨电极电解500mLNaNO3和Cu(NO3)2的混合溶液。通电一段时间后,阴、阳两极逸出的气体在标准状况下的体积分别为11.2L和8.4L,求原溶液中Cu2+的物质的量浓度(假设溶液的体积不变) A.1.25 mol•L-1 B.2.5 mol•L-1 C.0.50 mol•L-1 D.1.0 mol•L-1
12、下列叙述正确的是
A.0.1mol·L-1氨水中,c(OH-)=c(NH4+)
B.在常温下,10mL 0.02mol·L-1HCl溶液与10mL 0.02mol·L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
C.在0.1mol·L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
D.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A).
11、已知外电路中,电子由铜流向a极。有关下图所示的装置分析合理的一项是
 A.该装置中Cu极为正极
B.当铜极的质量变化为12 .8g时,a极上消耗的O2在标准状况下的体积为2.24L
C.b极反应的电极反应式为:H2-2e-=2H+
D.一段时间后锌片质量增加
A.该装置中Cu极为正极
B.当铜极的质量变化为12 .8g时,a极上消耗的O2在标准状况下的体积为2.24L
C.b极反应的电极反应式为:H2-2e-=2H+
D.一段时间后锌片质量增加
10、某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质。放电时的电池反应为:Li+LiMn2O4==Li2Mn2O4。下列说法正确的是
A.放电时,LiMn2O4发生氧化反应
B.放电时,正极反应为:Li++LiMn2O4+e-=Li2Mn2O4
C.充电时,LiMn2O4发生氧化反应
D.充电时,阳极反应为:Li++e-==Li
9、有体积相同、相等pH的烧碱溶液和氨水,下列叙述中正确的是
A. 两溶液物质的量浓度相同 B. 用同浓度的盐酸中和时,消耗盐酸的体积不相同
C.两溶液中OH-离子浓度相同 D. 加入等体积的水稀释后,pH仍相等
8、X、Y、Z、M代表四种金属元素.金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+ 和Z2+ 离子共存的溶液时,Y先析出;又知M2+ 离子的氧化性强于Y2+ 离子.则这四种金属的活动性由强到弱的顺序为 ( ) A .X>Z>Y>M B.X>Y>Z>M C. M>Z>X>Y D. X>Z>M>Y
7、用已知浓度的盐酸滴定未知浓度的NaOH溶液会导致测得的NaOH溶液浓度偏高的是
A.滴定时达到滴定终点时俯视读数
B.碱式滴定管量取NaOH溶液时,未进行润洗操作
C.滴定前滴定管中有气泡,滴定后消失
D.锥形瓶取用NaOH待测液前加少量水洗涤
6、250C时,某溶液中由水电离出的c(OH-)=1×10-13 mol/L,该溶液中一定不能大量共存的离子组是( )
A. NH4+ 、Fe3+ 、SO42- 、Cl- B. CO32- 、PO43- 、K+ 、Na+
C. Na+ 、SO42- 、NO3- 、Cl- D. SO42- 、 Na+ 、 HCO3- 、K+
5、为了除去MgCl2酸性溶性中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后再加入适量盐酸.这种试剂是
A.NH3·H2O B.NaOH C.Na2CO3 D.MgCO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com