
题目列表(包括答案和解析)
26.(10分)大家知道:Cu+H2SO4(稀)= Cu SO4+H2通常不能反应。请回答:
(1)试说明此反应在一般情况下不能发生反应的原因是____________________。
(2)若向稀H2SO4溶液中通入热的空气,则会发现铜会逐渐溶解。试写出有关反应的化学方程式________________________________________
(3)根据你所学过的知识,设法使其中的反应能发生,具体的方法是:________________
____________________________________;反应原理是:
阳极___________________________________________
阴极___________________________________
25.分别取等体积的pH=11和pH=12氨水,用一定物质的量浓度的H Cl溶液中和,则消耗H Cl溶液的体积之比( )
A.等于10 B.大于10 C.小于1/10 D.等于1
24.在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气。下列说法正确的是( )
A.甲烧杯中放入锌的质量比乙烧杯中放入锌的质量大 B.甲烧杯中的酸过量
C.反应速率:甲〉乙 D.反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)小
23.在pH=1的溶液中,可以大量共存的离子是 ( )
A.K+、Na+、SO42-、S2O32- B.NH4+、Mg2+、SO42-、Cl-
C.Na+、K+、HCO3-、Cl- D.K+、Na+、AlO2-、NO3
22.在相同温度时,100 mL 0.01mol/L的醋酸溶液与10 mL 0.1mol/L的醋酸溶液相比较,下列数值前者大于后者的是 ( )
A.中和时所需NaOH的量 B.H+的物质的量浓度
C.H+的物质的量 D.CH3COOH的物质的量[
21.甲酸的下列性质中,可以证明它是弱电解质的是 ( )
A.1mol/L甲酸溶液的c(H+)约为1×10-2mol/L B.甲酸能与水以任意比例互溶[
C.10mL 1mol/L甲酸恰好与10mL 1mol/LNaOH溶液完全反应
D.甲酸溶液的导电性比盐酸溶液的弱
20.水的电离过程为H2O H++OH-,在不同温度下其离子积为Kw(250C)=1.0×10-14,Kw(350C)=2.1×10-14,则下列叙述正确的是:
( )
H++OH-,在不同温度下其离子积为Kw(250C)=1.0×10-14,Kw(350C)=2.1×10-14,则下列叙述正确的是:
( )
A.c(H+)随着温度的升高而降低 B.在350C时,c(H+)>c(OH-)
C.水的电离常数Kw(250C)>Kw(350C) D.水的电离是一个吸热过程
19.在 的醋酸溶液中,存在平衡:
的醋酸溶液中,存在平衡: 下列说法正确的是( )
下列说法正确的是( )
A.加水稀释,电离程度增大,由 电离出来的
电离出来的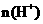 增大
增大
B.加入固体碳酸钠,平衡正向移动, 减小
减小
C.加入固体醋酸钠,平衡逆向移动, 均减小
均减小
D.加水稀释,中和此溶液所需的 NaOH溶液的体积增大
NaOH溶液的体积增大
18.物质的水溶液能导电,且该物质属于非电解质的是: ( )
A.溴化钠 B.三氧化硫 C.蔗糖 D.硫酸钡
17.高温下,某反应达平衡,平衡常数K= .恒容时,温度升高,H2浓度减小。下列说法正确的是 ( )
A.该反应的焓变为正值 B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小 D.该反应化学方程式为CO+H2O=CO2+H2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com