
题目列表(包括答案和解析)
5.可以证明次氯酸是弱酸的是 ( )
A.次氯酸可以与碱反应 B.次氯酸具有漂白性
C.漂白粉因在空气中久置而失效 D.次氯酸见光分解
4.向100mLNaOH溶液中通入标况下的CO21.12L后,将溶液小心蒸干后得到不含结晶水的固体5.08g,则下列说法中正确的是 ( )
A.原NaOH溶液的浓度是1.00mol/L,所得固体是Na2CO3;
B.原NaOH溶液的浓度是0.500mol/L,所得固体是Na2CO3和NaHCO3;
C.原NaOH溶液的浓度是1.00mol/L,所得固体是Na2CO3和NaOH;
D.原NaOH溶液的浓度是0.900mol/L,所得固体是Na2CO3和NaHCO3
3.下列物质的存放方法正确的是 ( )
A.固体碘放在棕色细口瓶中
B.盛放液溴的试剂瓶中常加入一些水
C.金属钠保存在四氯化碳中
D.新制的氯水置于无色的细口瓶中
2.下列说法正确的是 ( )
A.欲除去CO2中混有的HCl气体,可通过足量的饱和NaHCO3溶液
B.欲除去O2中混有的N2气体,可通过足量灼烧的CuO
C.欲除去HCl中混有的Cl2气体,可通过足量的AgNO3溶液
D.欲除去CO中混有的CO2气体,可通过足量Na2O2固体
1.某元素单质跟浓硝酸反应,参加反应的单质与硝酸的物质的量之比为1∶4,浓硝酸被还原为NO2 ,则该元素在反应产物中显示的化合价可能是 ( )
A.+1 B. +2 C. +3 D.+5
22.(13分)下图表示有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物(反应条件图中已省略)。
(1)A、D、F所代表物质的化学式分别为 、 、 。
(2)反应①中A恰好完全反应,C过量,写出该反应过程的所有化学方程式
。
(3)反应②中,若参加反应的B与F 的物质的量之比为3∶2,则生成的G与H物质的量之比为 。
(4)反应④的离子方程式是 。
(5)写出溶液乙与浓的氯化镁溶液混合时所发生反应的离子方程式
。
高二化学上综合练习(二)
一单选题(本题共10小题,每题只有一个选项符合题意,每小题2分,共20分)
21.(10分)某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的强酸、强碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
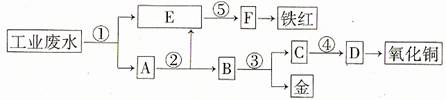
填写下面空白:
(1)图中标号处需加入的相应物质的名称分别是① 、② 、 ③ 、④ 。
(2)写出上述流程中与Au3+有关的离子方程式 。
(3)写出③处发生反应的化学方程式 。
(4)写出铁红与足量HI溶液反应的离子方程式 。
20.(10分)明矾在常温下是一种无色透明的晶体,它是医学上的常用药物,可用于治疗高血脂、溃疡等病症。明矾在其它领域也有着广泛应用。
(1)明矾的化学式是 。
(2)明矾可用作净水剂,用一个离子方程式表示其原理 。
(3)泡沫灭火器内所装的溶液可以选择明矾溶液和NaHCO3溶液,写出这两种溶液混合时所发生反应的离子方程式 。
(4)向明矾溶液中逐滴滴加Ba(OH)2溶液至产生沉淀的质量达到最大值,用一个离子方程式表示该过程发生的反应 。
(5)向 50 mL 1 mol/L明矾溶液中加入一定体积1.5 mol/L NaOH溶液,充分反应后产生 1.56 g沉淀,则加入NaOH溶液的体积可能为 mL。
19.(11分)硫酸被人们誉为“化学工业之母”,在国民生产中发挥着重要作用,硫酸的产量是衡量一个国家化学工业水平的标志。工业上生产硫酸包括三步:
(1)第一步,在沸腾炉中煅烧黄铁矿,反应如下:4FeS2+11O2 8SO2+2Fe2O3,该反应的氧化产物是 ,当生成8 mol SO2时转移电子的物质的量为 。
(2)第二步,在接触室中发生如下反应:2SO2+O2 2SO3。某科技小组的同学在一个恒温恒容的容器中模拟该反应,他们分两次进行实验,第一次向容器中加入2 mol SO2、1 mol O2,反应达平衡后测得SO2的转化率为α1,第二次向容器中加入3 mol SO2、1.5 mol O2, 反应达平衡后测得SO2的转化率为α2,则α1 α2(填“大于”、“等于”或“小于”)。
(3)第三步,在吸收塔中将SO3转化成硫酸。硫酸是化学实验中的常用试剂:
①有Na、Mg、Al、Cu四种金属,若两两混合后取混合物14 g与足量稀硫酸反应,产生标准状况下H2 5.6 L,则此混和物的组合方式最多有 种。
②可用稀硫酸与FeS反应来制H2S,H2S的水溶液叫做氢硫酸,它是一种二元弱酸。现将0.1 mol/L H2S溶液与0.2 mol/L NaOH溶液等体积混合,所得混合液中的关系正确的是 。
a+)+c(H+)=c(HS-)+c(OH-)+2c(S2-) B. c(H2S) +c(HS-) +c(S2-) =0.1 mol•L-1
C.2 c(H2S) +c(HS-) + c(H+) = c(OH-) a+)=2 c(H2S) +2c(HS-) +2c(S2-)
18.将0.02 mol/L的HCN溶液与0.02 mol/L的NaCN溶液等体积混合,所得混合溶液中c (CN-)<c (Na+),则下列关系式正确的是
a+)>c (CN-)>c (HCN) >c (H+)>c (OH-)
a+)>c (HCN)>c (CN-)>c (OH-)>c (H+)
C.c (HCN) >c (Na+)>c (CN-)>c (OH-)>c (H+)
D.c (HCN) >c (Na+)>c (CN-)>c (H+)>c (OH-)
第Ⅱ部分(非选择题,共56分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com