
题目列表(包括答案和解析)
23.(11分)已知某金属X有下列相关信息:①它的主要矿物的化学成分是X2O3;②它主要通过热还原法冶炼而成;③它的年产量位于金属之首。
(1)据此推断X是 (填选项字母)。
A.钛 B.铁 C.铝 D.铜
(2)在高炉中用含X2O3的矿物冶炼该金属的原理是
(用化学方程式表示)。
(3)电化学腐蚀是金属腐蚀的主要原因。当两种活泼性不同的金属在潮湿的环境中接触时,因形成原电池,活泼性强的金属首先被腐蚀。利用这一原理,为了保护轮船的钢质外壳,通常在行驶的轮船外壳上连接_____ _______ (填“铜板”、“锌板”)。
(4)为了满足某些尖端技术发展的需要,人们又合成了许多新型合金材料。储氢合金是一类能够大量吸收H2,并与H2结合成金属氢化物的材料。此过程发生了____________变化(填“物理”、“化学”),储氢合金属于__________ (填“纯净物”、“混合物”)。
(5)根据铁、铜、铝三种金属的活动顺序判断下列化学方程式正确的是 (填序号)。
①3Fe+2AlCl3=3FeCl2+2Al ②3Cu+2AlCl3=3CuCl2+2Al ③Fe+CuCl2=FeCl2+Cu
(6)某实验室废液中含有HCl、FeCl2和CuCl2等物质,若向其中加入稍过量的铁粉,充分反应后过滤,则滤渣中含有 (填化学式)。
(7)同学们设计了如下实验方案测定该矿物中X2O3的质量分数(装置气密性良好;矿物中的杂质不参加反应;假设矿物样品中的X2O3完全反应):
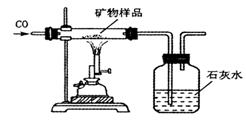 ①取矿物样品并称量该样品的质量;
①取矿物样品并称量该样品的质量;
②测出反应前广口瓶和瓶内物质总质量;
③测出反应后广口瓶和瓶内物质总质量;
④计算得出矿物样品中x2O3的质量分数。
你认为,该实验方案 (填“一定”或
“不一定”)能准确测出矿物中X2O3的质量分数,理由是 。
不改变装置和药品,你还可以通过测定哪些数据,再通过计算得出矿物中X2O3的质量分数: 。
从环保角度看,该装置的不足之处是 。
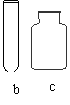
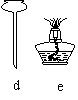
22.(8分)实验室有如下的实验仪器。请回答下列问题:
 |
|||||||||||||
 |
|||||||||||||
 |
|||||||||||||
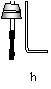 |
|||||||||||||
 |
|||||||||||||
|
|||||||||||||
|
|||||||||||||

①选择上图中的仪器组装一套加热固体制取氧气并用排水法收集的实验装置:
(填仪器序号),制气时该装置内反应的化学方程式:
。
②要确保用排水法收集到的氧气较纯,收集时要注意的两点是:
;
。
(2)为得到纯净干燥的CO2,将实验室中制得的CO2依次通过如下装置:
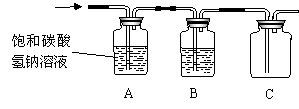
①装置A的作用: 。
②装置B内装的药品是: 。
③将点燃的镁条伸进集满CO2的集气瓶C中,镁条剧烈燃烧,瓶内有白色和黑色两种固体物质生成,反应的化学方程式: 。
通过该实验你得到的一点启发是: 。
21.(6分)分类法是学习化学的重要思想方法,依据同类物质性质的相似性,可以帮助我们做到举一反三。
现有下列三组物质:
A.空气、胆矾、冰水、蔗糖
B.KOH、H2SO4、Ca(OH)2、Ba(OH)2
C.NH4Cl、Na2CO3、SO2、Na2SO4
(1)填写下表空白
|
组 别 |
A组 |
B组 |
C组 |
|
分类标准 |
纯净物 |
碱 |
|
|
不属于上述分类标准的物质 |
空气 |
|
 SO2 SO2 |
(2)请仿照检验CO2的反应,选用SO2 或SO3书写一个类似的化学反应方程式 。
(3)NH4Cl溶液与KOH溶液能够反应,实质是因为它们在水中解离出来的NH4+和OH-结合生成了NH3和H2O。结合发生复分解反应的条件,请回答:Ba(OH)2溶液与Na2SO4溶液能够反应的实质是它们在水中解离出 离子结合生成了 。
(4)请依据(3)中获得的启示,判断下列在水溶液中能大量共同存在的一组离子是 。
A.H+、OH- B.CO32-、H+ C.Cu2+、OH- D.Na+、Cl-
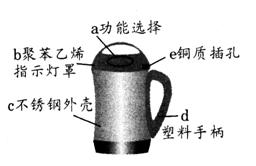
20.(10分)通过学习,我们可以从化学的角度看问题。豆浆机由于快捷方便而进入千家万户,请根据图示回答:
(1)制作材料中属于金属或合金的是
(选填一种物质编号),属于有机合成材料的是 (选填一种物质编号);
(2)制作手柄的塑料属于 塑料(填“热塑性”或“热固性”);
(3)豆浆已成为众多家庭的早餐饮品,以下是豆浆中一些营养成分的平均质量分数。请根据下表回答:
|
成分 |
水 |
蛋白质 |
脂肪 |
糖类 |
钙 |
磷 |
铁 |
维生素A |
|
质量分数/% |
96.0 |
1.8 |
0.7 |
1.1 |
0.01 |
0.03 |
0.0005 |
0.015 |
①豆浆中含有的微量元素是 ;
②青少年缺乏 元素易患有佝偻病。
③在豆浆所含的营养素中能供给人体能量的营养素有 。
④若成年人每天食用100g豆浆,则摄入蛋白质的质量为 g。
纤维素的化学式为(C6H10O5)n,在催化剂和加热的条件下纤维素可以与水反应生成葡萄糖,写出该反应的化学方程式 。
⑤人体缺乏维生素C会引发_______ ____病。维生素C的相对分子质量为176,维生素C中C、H、O三种元素的质量比为9∶1∶12,则维生素C的化学式为 。
19.(4分)许多无明显现象的化学反应可通过滴加其它试剂的方法,使之产生明显的现象 以证明反应确实发生了。例如以下几个实验:

(1)实验甲中的NaOH与HCl恰好反应时,可观察到的现象是_____________________;
(2)从研究原理得知,实验甲是通过检验反应前后溶液酸碱性的改变证明反应发生了,与之采用相同原理的还有实验__________________(填“乙”或“丙”);
 (3)证明实验丙中NaOH与CO2发生了反应,除了可以滴加酸,还可滴加的试剂是______
________
(4)若将含有盐酸的氯化钙溶液中和到中性,在不用指示剂的情况下,加入的试剂可以是__ ______
(写化学式)。
(3)证明实验丙中NaOH与CO2发生了反应,除了可以滴加酸,还可滴加的试剂是______
________
(4)若将含有盐酸的氯化钙溶液中和到中性,在不用指示剂的情况下,加入的试剂可以是__ ______
(写化学式)。
18.(2分)化肥和农药是关系农业生产的两类重要物质。现有NH4HC O3、CuCl2、KNO3、CuSO4四种物质,其中属于复合肥的是 ,常用来制农药的是 。
17.(2分)某粒子结构示意图为 ,该粒子的核电荷数为____________;当a=_______时, 表示的是阳离子结构示意图。
16.在密闭容器中,将少量乙醇(化学式C2H5OH)置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质W。现测得反应前后各物质的质量如下:
|
物质 |
乙醇 |
氧气 |
二氧化碳 |
水蒸气 |
W |
|
反应前质量/g |
48 |
80 |
0 |
0 |
0 |
|
反应后质量/g |
2 |
0 |
44 |
54 |
x |
下列有关说法错误的是: ( )
A.W物质一定含有氢元素 B.该反应属于氧化反应
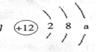 C.W物质一定含有氧元素
D.x的值为28
C.W物质一定含有氧元素
D.x的值为28
15.已知某两种物质在一定条件下能发生如下图所示的反应,则下列说法正确的是( )

A.该图示符合质量守恒定律 B.图中反应物均为化合物
C.该反应属于置换反应 D.图示中反应物和生成物的原子数不相等
14.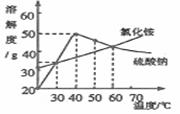 图为氯化铵和硫酸钠的溶解度曲线。下列说法中不正确的是 ( )
图为氯化铵和硫酸钠的溶解度曲线。下列说法中不正确的是 ( )
A.30℃时,氯化铵、硫酸钠的溶解度相同
B.氯化铵的溶解度随温度的升高而增大
C.将50℃时硫酸钠的饱和溶液降低温度,始终有晶体析出
D.将60℃时硫酸钠的饱和溶液降温至40℃,溶质的质量分数不变
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com