
题目列表(包括答案和解析)
22.(9分)某研究小组将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50 mL)。回答下列问题:

(1)研究小组做该实验时环境温度 (填“高于”、“低于”或“等于”)22 ℃,判断的依据是
(2)由题干及图形可知,V1/V2= : 时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为 mol/L。
(3)若通过实验测定及有关计算知酸碱恰好完全中和时共放出Q KJ的热量,请写出此反应的热化学方程式:
21.(5分)废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末。
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是 (填字母)。
A.热裂解形成燃油 B.露天焚烧
C.作为有机复合建筑材料的原料 D.直接填埋
(2)用 的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
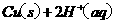 ====
====

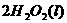 ====
====

 ====
==== 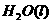

在 溶液中
溶液中 与
与 反应生成
反应生成 和
和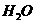 的热化学方程式为
的热化学方程式为
。
(3)在298K下,C、Al的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。又知一定条件下,Al能将C从CO2置换出来,写出此置换反应的热化学方程式
20.(2分)已知:下列两个热化学方程式:
Fe(s) + 1/2O2(g)  FeO(s)
FeO(s)  =-272.0KJ/mol
=-272.0KJ/mol
2Al(s) + 3/2O2(g)  Al2O3(s)
Al2O3(s)
 =-1675.7KJ/mol
=-1675.7KJ/mol
则 Al(s)的单质和FeO(s)反应的热化学方程式_____________________________________。
19.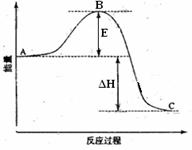 (13分)2SO2(g)+O2(g)
=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH = - 99kJ·mol-1。请回答下列问题:
(13分)2SO2(g)+O2(g)
=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH = - 99kJ·mol-1。请回答下列问题:
(1)图中A、C分别表示 、
,E的大小对该反应的反应热 (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点
(2)图中△H= KJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化为V2O5。写出该催化循环机理的化学方程式
、 (4)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H(要求计算过程)。
18.(6分)常温常压下,断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为KJ.mol-1)下表是一些键能数据(KJ·mol-1)
|
化学键 |
键能 |
化学键 |
键能 |
化学键 |
键能 |
化学键 |
键能 |
|
C-H |
414 |
C-F |
489 |
H-F |
565 |
F-F |
158 |
|
H-H |
436 |
H-N |
391 |
|
|
|
|
(1)根据键能数据计算以下反应的反应热△H:
CH4(g)+4F2(g)﹦CF4(g)+4HF(g) △H
(2)根据键能和反应热化学方程式 1/2N2(g)+3/2H2(g) = NH3(g ) △H = -46 kJ·mol-1 计算N≡N的键能。
17.在理论上不能用于设计原电池的化学反应是
B. HCl ( aq ) + NaOH ( aq ) = NaCl ( aq ) + H2O ( l ) △H < 0
C. 2CH3OH ( l ) +3O2 ( g ) = 2CO2 ( g ) + 4H2O ( l ) △H < 0
D. 4Fe (OH)2 ( s ) + 2H2O ( l ) + O2 ( g ) = 4Fe (OH)3( s ) △H < 0
E. 2H2 ( g ) + O2 ( g ) = 2H2O ( l ) △H < 0
16.已知299 K时,合成氨反应 N2 (g ) + 3H2 (
g ) 2NH3 ( g ) △H = -92.0
kJ/mol,将此温度下的1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
2NH3 ( g ) △H = -92.0
kJ/mol,将此温度下的1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
A. 一定大于92.0 kJ B. 一定等于92.0 kJ C. 一定小于92.0 kJ D. 不能确定
15.已知:2CO(g)+O2(g)=2CO2(g) ΔH =  566 kJ/mol
566 kJ/mol
 Na2O2(s)+CO2(g)=Na2CO3(s)+
Na2O2(s)+CO2(g)=Na2CO3(s)+
 ΔH=
ΔH= 226 kJ/mol
226 kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为566 kJ/mol
B.右图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH =  452 kJ/mol
452 kJ/mol
D.CO2(g)与Na2O2(s)反应放出452kJ热量时,电子转移数为1.204×1024(个)
14. 灰锡(常温下以粉末状存在)和白锡是锡的两种同素异形体。
已知:①Sn(s,白)+2HCl(aq)== SnCl2(aq)+H2(g) ΔH1
②Sn(s,灰)+2HCl(aq)== SnCl2(aq)+H2(g) ΔH2
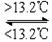 ③Sn(s,灰) Sn(s,白) ΔH3 = +2.1 kJ·mol-1
③Sn(s,灰) Sn(s,白) ΔH3 = +2.1 kJ·mol-1
下列说法正确的是( )
A.ΔH1>ΔH2
B.锡在常温下以灰锡状态存在
C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处在低于13.2 ℃的环境中,会自行毁坏
13. 下列热化学方程式正确的是(注: 的绝对值均正确)( )
的绝对值均正确)( )
A.C2H5OH(l)+3O2(g)==2CO2(g) +3H2O(g);△H= -1367.0 kJ/mol(燃烧热)
B.NaOH + HCl == NaCl + H2O;△H= -57.3kJ/mol(中和热)
C.S(s) + O2(g) == SO2(g);△H= -269.8kJ/mol(反应热)
D.2NO2==O2+2NO;△H= +116.2kJ/mol(反应热)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com