
题目列表(包括答案和解析)
18. (16分)短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):
(16分)短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):

(1)X的电子式是 ;甲分子的空间结构呈 形。
(2)工业合成甲,综合考虑各种因素所选择的条件是:
(3)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。
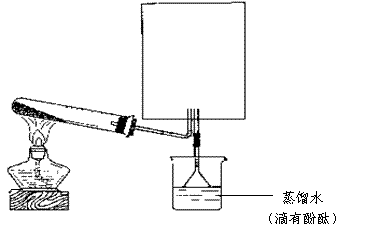
①在图中方框内绘出用烧瓶收集甲的仪器装置简图。
②试管中的化学反应方程式为 。
③烧杯中溶液由无色变为红色,其原因是(用电离方程式表示)
。
(4)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是 。
(5)n mol丁与n mol丙在一定条件下反应,生成4n mol乙和另一化合物,该化合物蒸气的密度是相同状况下氢气的174倍,其化学式是 。
17.(18分)
 (1)将固体NH4I置于密闭容器中,某温度下发生下列变化: NH4I(固 )
(1)将固体NH4I置于密闭容器中,某温度下发生下列变化: NH4I(固 ) NH3(气) + HI(气), 2HI(气)
NH3(气) + HI(气), 2HI(气)  H2(气) + I2(气)当反应达到平衡时c(H2)= 0.5 mol/L, c(HI)= 4 mol/L, 则
H2(气) + I2(气)当反应达到平衡时c(H2)= 0.5 mol/L, c(HI)= 4 mol/L, 则
c(NH3)为 HI 的分解率为 。
(2)右图表示在某温度下经时间t反应后,物质 X、Y、Z、W 的物质的量的大致变化情况。则所发生反应的化学方程式是____________________________
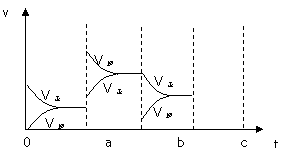 (3)右图表示在密闭容器中:2SO2+O2
(3)右图表示在密闭容器中:2SO2+O2 2SO3(正反应放热)达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a
点改变的条件可能是 ;b点改变的条件可能是 ;若c点增大压强时,画出反应速度变化情况。
2SO3(正反应放热)达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a
点改变的条件可能是 ;b点改变的条件可能是 ;若c点增大压强时,画出反应速度变化情况。
16.(6分)配平下列化学(或离子)方程式并标明电子转移情况:
(1) Cu2S + HNO3 -- Cu(NO3)2+ NO ↑ + H2SO4+ H2O
(2) SO3 + MnO4
+ MnO4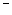 + H
+ H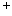 -- Mn
-- Mn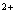 + SO4
+ SO4 + H2O
+ H2O
15.在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g)。
nY(g)。
反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
  气体体积/L
气体体积/L温度 c(Y)/mol·L-1 |
1 |
2 |
3 |
|
100 |
1.00 |
0.75 |
0.53 |
|
200 |
1.20 |
0.90 |
0.63 |
|
300 |
1.30 |
1.00 |
0.70 |
下列说法正确的是
A.m>n
B.正反应为放热
C.温度不变,压强增大,Y的质量分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
14.2.0molPCl3和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下列反应:PCl3(g)+Cl2(g)  PCl5(g);达平衡时,PCl5为0.40mol。如果此时移走1.0mol
PCl3和0.50molCl2,在相同条件下再达平衡时,PCl5的物质的量是
PCl5(g);达平衡时,PCl5为0.40mol。如果此时移走1.0mol
PCl3和0.50molCl2,在相同条件下再达平衡时,PCl5的物质的量是
A.0.40mol B.小于0.20mol
C.0.20mol D.大于0.20mol,小于0.40mol
13.为了防止NO、NO2、N2O4对大气的污染,常采用氢氧化钠溶液吸收处理(方程式:2NO2+2NaOH==NaNO3+NaNO2+H2O;NO2+NO+2NaOH== 2NaNO2+H2O)。
现有由amolNO、bmol NO2、cmolN2O4组成的混合气体恰好被VL氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度最小为
a+b+c 2(a+b+c)

 A. mol·L-1
B.
mol·L-1
A. mol·L-1
B.
mol·L-1
V 3V
a +b+2c b+2c

 C.
mol·L-1
D.
mol·L-1
C.
mol·L-1
D.
mol·L-1
V V
11.对于mA(g)+nB(g) pC(g)+ qD(g)的平衡体系,当升高温度时,体系
pC(g)+ qD(g)的平衡体系,当升高温度时,体系
的平均相对分子质量对氢气的相对密度从16.5变成16.9,则下列说法正确的是
A.m+n>p+q 正反应是放热反应 B.m+n>p+q 正反应是吸热反应
C.m+n<p+q 逆反应是放热反应 D.m+n = p+q 逆反应是吸热反应
 A.α1减小,α2增大
B.α1、α2均增大
A.α1减小,α2增大
B.α1、α2均增大
C.α1、α2均减小 D.α1增大,α2减小
10.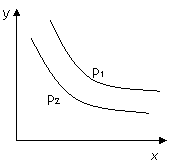 反应:L(s)+aG(g)
反应:L(s)+aG(g) bR(g) 达到平衡时,
bR(g) 达到平衡时,
温度和压强对该反应的影响如右图所示:图中压强p1>p2,
x轴表示温度,y轴表示平衡混合气中G的体积分数。
则下列说法正确的是
A.定温时,加压平衡不移动 B.该反应正反应吸热
C.a>b D.定压时,升温平衡不移动
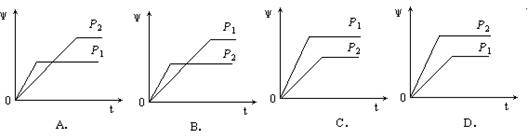
9.在一定温度不同压强(P1<P2)下,可逆反应2X(g)  2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是B
2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是B
8. 下列说法错误的是
下列说法错误的是
A.浓氨水中加NaOH固体产生氨气,它是溶解平衡逆向移动的结果
B.X(s)+aY(g) bZ(g)反应达到平衡后,增加X,平衡不移动
bZ(g)反应达到平衡后,增加X,平衡不移动
C.Na2S2O3溶液和盐酸反应时,加热可加快反应速率
D.KSCN溶液和FeCl3溶液混合,反应达平衡后,滴加KCl溶液可使平衡逆向移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com