
题目列表(包括答案和解析)
30.(7分)下列用字母表示的是初中化学常见的物质,可能由H、C、O、Na、S、Ca、Fe中的几种元素组成。
(1)A是一种氧化物,可用做干燥剂,可用于生成改良酸性土壤的碱B,则A→B的化学方程式为 。
(2)C和D发生中和反应生成E和F,C、D、E均含有3种元素,F电解可生成两种气体,写出中和反应的化学方程式 及电解F的化学方程式 。
(3)G既能与稀盐酸反应生成M,又能与氢氧化钙溶液反应生成C,且M 与C能反应,则G的化学式为 (写一种即可),M和C反应的化学方程式为 。
(4)从上述物质中任选2种为一组,按下图所示装置进行实验。一木块漂浮于X中,向X中缓 缓加入(或通入)少量物质Y后最终木块上浮。
 友情提示:填写物质的化学式、名称或俗称。
友情提示:填写物质的化学式、名称或俗称。
|
|
① |
② |
③ |
④ |
|
X |
|
|
|
|
|
Y |
|
|
|
|
29. (6分)随着经济的发展,环境成为是人们日益关注的问题。
(1)为了降低大气中二氧化碳的含量,化学家们正想尽办法用化学反应的手段使二氧化碳“变废为宝”。用三甲基膦做催化剂,在高压、极低温度条件下,CO2和H2可以高效合成甲酸(HCOOH),并实现了工业化生产。该反应的化学方程式为____________。
(2)目前使用膜分离法从空气中分离出CO2,这个过程中CO2发生了________ (填“物理”或“化学”)变化。
(3)2011年3月,日本福岛第一核电站发生核辐射泄漏。堆芯熔毁是核电事故中最严重的事态。福田第一核电站机组反应堆芯放出氢气,当接触外界的氧气发生剧烈反应,导致连续爆炸。请写出氢气爆炸时的化学方程式__________。
(4)当空气受SO2严重污染时,可通过飞机喷洒X粉末,使空气中的SO2含量明显降低,该过程发生的反应是2X+2SO2+O2 2CaSO4+2CO2。X的化学式是__________。
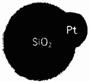 (5)纳米球异质二聚体是纳米自动化产业中的一种新模型(如图所示),它可望用于河流和溪水的污染控制。不溶于水的二氧化硅晶体可以制成微小的纳米球。在铂的催化作用下,双氧水分解,同时使一个二氧化硅纳米球与一个铂纳米球相结合。根据以上信息判断,下列有关说法错误的是__________。
(5)纳米球异质二聚体是纳米自动化产业中的一种新模型(如图所示),它可望用于河流和溪水的污染控制。不溶于水的二氧化硅晶体可以制成微小的纳米球。在铂的催化作用下,双氧水分解,同时使一个二氧化硅纳米球与一个铂纳米球相结合。根据以上信息判断,下列有关说法错误的是__________。
A.二氧化硅纳米球中含有的硅、氧原子个数比为1:2
B.纳米球异质二聚体,其微粒大小在纳米级范围
C.双氧水分解时,二氧化硅是催化剂
D.因为二氧化硅晶体能与水反应而溶解,所以该纳米级发动机可以用于水污染的控制
28. (6分)我国属于海洋大国,浩瀚的海域蕴藏着丰富的化学资源。
(1)海底蕴藏着大量的煤、 、天然气等常规化石燃料。
(2)天然气的主要成分是甲烷(CH4),可直接用作气体燃料。燃烧反应前后分子种类变化的微观示意图如下所示。
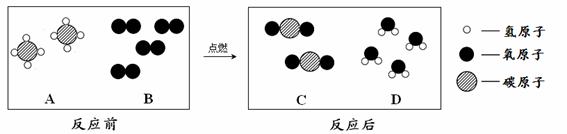
① 1个B分子中含有 个原子。
② 四种物质中属于化合物的是 (填图中字母)。
③ 若8gA参加反应,则生成C的质量为 g。
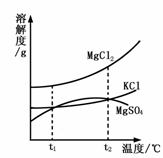 (3)海水晒盐能够得到粗盐和卤水。卤水中含有MgCl2、KCl和MgSO4等物质,右图是它们的溶解度曲线。t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是 。将t1℃的MgCl2、KCl和MgSO4三种物质的饱和溶液加热到t2℃以上时,可能会析出
晶体。
(3)海水晒盐能够得到粗盐和卤水。卤水中含有MgCl2、KCl和MgSO4等物质,右图是它们的溶解度曲线。t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是 。将t1℃的MgCl2、KCl和MgSO4三种物质的饱和溶液加热到t2℃以上时,可能会析出
晶体。
27. (6分)铁、铜是我们生活中重要的金属材料。
(1)将油漆涂在铁艺家具上防止生锈,其目的是将铁与空气中的 隔绝。
(2)工业上用一氧化碳和赤铁矿(主要成分是氧化铁)冶炼铁,发生的化学方程式为 。
(3)矿物的储量有限,而且不可再生,我们必须保护金属资源并进行金属的回收利用。欲从含有硫酸、硫酸亚铁和硫酸铜的废液中,回收全部铜。处理过程如下:
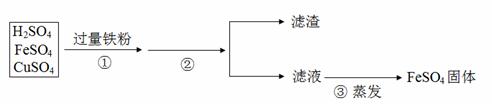
步骤①加入过量铁粉,发生的反应方程式为: , 。充分反应后步骤②进行的操作是 ,得到的滤渣中含有 ,继续处理可以得到纯净的金属铜和硫酸亚铁固体。
26.(5分)化学与生活息息相关。
(1)苦笋是竹笋的一类,被人们称为笋中珍品。下表列出的是每100g某苦笋含有的部分营养成分:
|
营养成分 |
蛋白质 |
维生素C |
纤维素 |
钙 |
镁 |
磷 |
锌[] |
|
含 量 |
2.6g |
5mg |
1.8g |
9mg |
1mg |
64mg |
0.33mg |
①表中的“磷”指的是
(填“元素”或“分子”),已知它的原子结构示意图为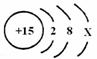 ,则X为
;
,则X为
;
 ② 蛋白质、维生素C和纤维素均属于 (填“有机物”或“无机物”);
② 蛋白质、维生素C和纤维素均属于 (填“有机物”或“无机物”);
③ 维生素C的化学式为C6H8O6,则维生素C中H、O元素的质量比为 。
(2)禁止燃放孔明灯,因为孔明灯燃烧时外焰温度高达300多度,一旦飘落到加油站、 液化气站、油库等地,孔明灯会 而引发火灾。(填字母)
A.提供可燃物 B.供给氧气 C.使温度达到可燃物的着火点
25. 在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系能用右下图曲线表示的是
|
序号 |
甲 |
乙 |
|
① |
HCl溶液 |
NaOH溶液 |
|
② |
HCl溶液 |
大理石 |
|
③ |
H2SO4溶液 |
锌粒 |
|
④ |
Ca(OH)2溶液 |
Na2CO3溶液 |
|
⑤ |
CuSO4溶液 |
铁粉 |
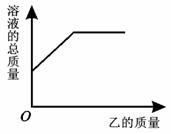
A.①② B.③④ C.①⑤ D.②③
23. 下列是分析已变质氢氧化钠溶液的相关实验,其中合理的是
|
序号 |
实验目的 |
实验过程 |
|
① |
除去杂质 |
取溶液,滴加石灰水至恰好完全反应,过滤 |
|
② |
确定成分 |
取少量溶液,加入石灰水,过滤,向滤液中滴加酚酞溶液 |
|
③ |
证明变质 |
取少量溶液,滴加盐酸,将生成的气体通入澄清的石灰水 |
|
④ |
测定纯度 |
取一定量溶液,加入盐酸,用氢氧化钠固体吸收气体,称量 |
A.②③ B.①③ C.②④ D.①④
|
|
②2NO+O2 2NO2
③3NO2+H2O 2HNO3+NO,下列判断不正确的是
A. ②为化合反应
B. 一氧化氮(NO)的化学性质稳定
C. 上述含氮物质中氮元素的化合价有-3,+2,+4,+5
D. 制取硝酸过程中产生的NO可循环使用
22. 下列质量增加的变化中有一种与其他三种存在着本质的区别,这种变化是
A.长期放置在空气中的氢氧化钠质量增加
B.久置在潮湿空气中的铁钉质量增加
C.久置在空气中的生石灰质量增加
D.长期敞口放置的浓硫酸质量增加
21.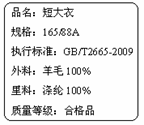 右图是某短大衣标签的部分内容,下列有关认识不正确的是
右图是某短大衣标签的部分内容,下列有关认识不正确的是
A. 短大衣是由两种材料制成的
B. 羊毛和涤纶均属于有机高分子材料
C. 涤纶属于天然纤维
D. 可以通过灼烧来区别涤纶和羊毛
20. 将下列固体分别放入水中,溶液温度明显降低的是
A.食盐 B.烧碱 C.生石灰 D.硝酸铵
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com