
题目列表(包括答案和解析)
8、对于反应A2+3B2=2C来说,以下化学反应速率的表示中,反应速率最快的是( )
A、v(B2)=0.8 mol/ (L·s) B、v(A2)=0.4 mol/ (L·s)
C、v(C)=0.6 mol/ (L·s) D、v(B2)=4.2 mol/ (L·min)
7、下列离子方程式中正确的是( )
A、Cu(OH)2与盐酸反应:H+ + OH-=H2O
B、氨气通入醋酸溶液中:NH3 + CH3COOH=CH3COO-+NH4+
C、MgSO4溶液与Ba(OH)2溶液反应:SO42-+Ba2+=BaSO4↓
D、CaCO3与稀盐酸反应:CO32-+2H+=H2CO3
6、下列各组离子一定能大量共存的是( )
A、在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN-
B、在使酚酞变红的溶液中:Na+、K+、AlO2-、CO32-
C、在水电离产生的c(OH-)=1×10-14mol·L-1的溶液中:NH4+、Al3+、SO42-、NO3-
D、在pH试纸变深红色的溶液中:K+、Fe2+、Cl-、NO3-
5、NA代表阿伏加德罗常数,以下说法正确的是( )
A、12lg CCl2F2所含的氯原子数为2NA
B、常温常压下l mol NO2气体与水反应生成NA个NO3一 离子
C、氯化氢气体的摩尔质量等于NA个氯原子和NA 个氢原子的质量之和
D、124g Na2O溶于水后所得溶液中含有O2-离子数为2NA
4、下列操作方法或实验装置正确的是( ) www.k@s@5@ 高#考#资#源#网

3、下列表示物质结构的化学用语或模型正确的是( )
A、8个中子的碳原子的核素符号:12C
B、HF的电子式:
C、Cl-离子的结构示意图: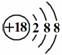 D、CH4分子的比例模型:
D、CH4分子的比例模型:
2、强弱电解质的本质区别是( )
A、导电能力 B、相对分子质量 C、电离程度 D、溶解度
1、常温下,下列变化过程不是自发的是( )
A、石灰石的分解 B、原电池产生电流
C、氯化铵晶体与氢氧化钡晶体反应 D、铁在潮湿空气中生锈
21、 (15分)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):
(15分)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):
CO(g)+2H2(g) 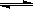 CH3OH(g)
CH3OH(g)
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K= ,升高温度,K值 (填“增大”、“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a 氢气的浓度减少 b 正反应速率加快,逆反应速率也加快
c 甲醇的物质的量增加 d 重新平衡时n(H2)/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: (用化学方程式表示)。
河南大学附属中学2010-2011学年上期期中考试试题
20、(12分)今有①盐酸 ②硫酸 ③醋酸三种酸:
(1)在同体积,同PH的三种酸中,分别加入足量的锌粉,在相同条件下产生H2的体积由大到小的顺序是____________
(2)在同体积、同浓度的三种酸中,分别加入足量的锌粉,在相同条件下产生H2的体积由大到小的顺序是____________
(3)物质的量浓度为0.1 mol·L-1的三种酸溶液的PH由大到小的顺序是____________ _;如果取等体积的0.1 mol·L-1的三种酸溶液,用0.1 mol·L-1的NaOH溶液中和,当恰好完全反应时,消耗溶液的体积由大到小的顺序是____________ ___(以上均用酸的序号填写)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com