
题目列表(包括答案和解析)
7.pH=3的两种酸溶液A、B,取等体积酸分别与足量的锌反应,酸A比酸B产生的氢气的量多.下列说法正确的是 ( )
A.A是强酸、B一定是弱酸 B.A是弱酸、B一定是强酸
C.A是强酸、B是强酸 D.A酸性一定比B酸性弱
6.已知:CO(g) + H2O(g) H2(g)
+ CO2(g)的平衡常数K随温度的变化如下表,下列说法正确的是( )
H2(g)
+ CO2(g)的平衡常数K随温度的变化如下表,下列说法正确的是( )
|
温度/℃ |
400 |
500 |
830 |
1000 |
|
平衡常数K |
10 |
9 |
1 |
0.6 |
A.正反应是吸热反应
B.恒温时增大压强,正反应速率增大
C.830℃时,反应达到平衡,c(CO)=c(CO2)
D.400℃时,恒容反应器中投入CO、H2O、H2、CO2物质的量分别为5 mol、1 mol、2 mol、3mol,反应向逆方向进行
5.已知反应mX(g)+nY(g)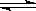 qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
A.通入稀有气体使压强增大,平衡将正向移动
B.X的正反应速率是Y的逆反应速率的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.若平衡时X、Y的转化率相等,说明反应开始时X、Y的物质的量之比为n:m
4.用蒸馏水稀释1 mol/L醋酸时,始终保持增大趋势的是( )
A.溶液中的c(CH3COO-) B.溶液中的c(H+)
C.溶液中的c(CH3COOH) D.溶液中的c(OH-)
3.一定温度下,在容积恒定的密闭容器中,进行如下可逆反应:
A(s)+2B(g) 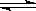 C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到
C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到
平衡状态的是 ( )
①混合气体的密度 ②容器内气体的压强
③混合气体的总物质的量 ④B的物质的量浓度
A.①④ B.②③
C.②③④ D.只有④
2.已知HCN(aq)与NaOH(aq)反应的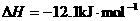 ;HCl(aq)与NaOH(aq)反应的
;HCl(aq)与NaOH(aq)反应的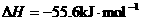 ,则HCN在水溶液中电离的
,则HCN在水溶液中电离的 等于 ( )
等于 ( )
A.
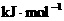 B.-43.5
B.-43.5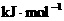
C.+43.5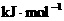 D.+67.7
D.+67.7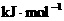 www.k@s@5@
高#考#资#源#
www.k@s@5@
高#考#资#源#
1.下列过程中化学反应速率的加快对人类有益的是 ( )
A.金属的腐蚀 B. 氨的合成 C.塑料的老化 D. 食物的腐败
25. 有机物A只含有C、H、O三种元素,常用作有机合成的中间体。 16.8 g该有机物经燃烧生成44.0 gCO2和14.4 gH2O;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O-H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1。 (1)通过计算确定该有机物A的分子式,并写出A的结构简式
(2)有机物B是A的同分异构体,1 mol B可与1mol Br2加成。该有机物所有碳原子在同一个平面,没有顺反异构现象。请写出B的结构简式是 。
 温州中学2010学年第一学期期中考试
温州中学2010学年第一学期期中考试
24.A、B两种烃的最简式相同,已知A完全燃烧后生成的CO2和H2O的物质的量之比为2:1,且A的相对分子质量为78。A不能使酸性KMnO4溶液褪色,也不与溴水反应,B能使这两种溶液褪色。在相同状况下,A与B蒸气的密度比为3:1。写出这两种烃的结构简式。
23.(9分)I.下列实验中仪器的下端必须插入反应物液面下的是: 。(填写序号)
 ① 制备氢气的简易装置中的长颈漏斗; ②制备氯气装置中的分液漏斗; ③制备硝基苯时的温度计; ④用乙醇制取乙烯时的温度计; ⑤分馏石油时的温度计。
① 制备氢气的简易装置中的长颈漏斗; ②制备氯气装置中的分液漏斗; ③制备硝基苯时的温度计; ④用乙醇制取乙烯时的温度计; ⑤分馏石油时的温度计。
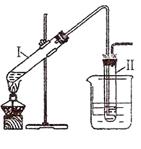
II.完成以下实验:①
用右图所示的装置制取溴乙烷;②进行溴乙烷的性质实验。在试管I中依次加入2 mL 蒸馏水、4 mL浓硫酸、2 mL 95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水。加热试管I至微沸状态数分钟后,冷却。试回答下列问题:
(1)试管I中反应的化学方程式 __________________。
(2)反应结束后,U形管中粗制的C2H5Br呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的_______________(填字母)
A.NaOH溶液 B.H2O C.Na2SO3溶液 D.CCl4
(3)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后__________________(填代号)。
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却
(4)在进行溴乙烷与NaOH乙醇溶液共热的性质实验时,把生成的气体通过下图所示的装置。
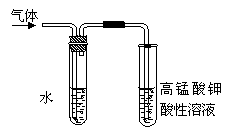
用上图装置进行实验的目的是 _;上图中右边试管中的现象是 ;水的作用是 。
(5)溴乙烷(C2H5Br)多一个碳的同系物在氢氧化钠的醇溶液中能发生反应,生成的产物为_________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com