
题目列表(包括答案和解析)
5、 碱和对应的碱性氧化物的联系:
① 碱性氧化物和碱都可跟酸反应生成盐和水:
CuO + 2HCl == CuCl2 + H2O
Cu(OH)2 + 2HCl == CuCl2 + 2H2O
CaO + 2HCl == CaCl2 + H2O
Ca(OH)2 + 2HCl == CaCl2 + 2H2O
②碱性氧化物跟水反应生成对应的碱:(生成的碱一定是可溶于水,否则不能发生此反应)
K2O + H2O == 2KOH Na2O +H2O == 2NaOH
BaO + H2O == Ba(OH)2 CaO + H2O == Ca(OH)2
③不溶性碱加热会分解出对应的氧化物和水:


 Mg(OH)2 == MgO + H2O Cu(OH)2 == CuO + H2O
Mg(OH)2 == MgO + H2O Cu(OH)2 == CuO + H2O
 2Fe(OH)3 == Fe2O3 + 3H2O 2Al(OH)3 == Al2O3 + 3H2O
2Fe(OH)3 == Fe2O3 + 3H2O 2Al(OH)3 == Al2O3 + 3H2O
4、 酸和对应的酸性氧化物的联系:
① 酸性氧化物和酸都可跟碱反应生成盐和水:
CO2 + 2NaOH == Na2CO3 + H2O(H2CO3 + 2NaOH == Na2CO3 + 2H2O)
SO2 + 2KOH == K2SO3 + H2O
H2SO3 + 2KOH == K2SO3 + 2H2O
SO3 + 2NaOH == Na2SO4 + H2O
H2SO4 + 2NaOH == Na2SO4 + 2H2O
② 酸性氧化物跟水反应生成对应的酸:(各元素的化合价不变)
CO2 + H20 == H2CO3 SO2 + H2O == H2SO3
SO3 + H2O == H2SO4 N205 + H2O == 2HNO3
(说明这些酸性氧化物气体都能使湿润pH试纸变红色)
3、 常见一些变化的判断:
① 白色沉淀且不溶于稀硝酸或酸的物质有:BaSO4、AgCl(就这两种物质)
② 蓝色沉淀:Cu(OH)2、CuCO3
③ 红褐色沉淀:Fe(OH)3
Fe(OH)2为白色絮状沉淀,但在空气中很快变成灰绿色沉淀,再变成Fe(OH)3红褐色沉淀
④沉淀能溶于酸并且有气体(CO2)放出的:不溶的碳酸盐
⑤沉淀能溶于酸但没气体放出的:不溶的碱
2、 一些特殊物质的颜色:
黑色:MnO2、CuO、Fe3O4、C、FeS(硫化亚铁)
蓝色:CuSO4•5H2O、Cu(OH)2、CuCO3、含Cu2+ 溶液、
液态固态O2(淡蓝色)
红色:Cu(亮红色)、Fe2O3(红棕色)、红磷(暗红色)
黄色:硫磺(单质S)、含Fe3+ 的溶液(棕黄色)
绿色:FeSO4•7H2O、含Fe2+ 的溶液(浅绿色)、碱式碳酸铜[Cu2(OH)2CO3]
无色气体:N2、CO2、CO、O2、H2、CH4
有色气体:Cl2(黄绿色)、NO2(红棕色)
有刺激性气味的气体:NH3(此气体可使湿润pH试纸变蓝色)、SO2
有臭鸡蛋气味:H2S
1、常见物质的颜色:多数气体为无色,多数固体化合物为白色,多数溶液为无色。
22. 3 g +216.1 g -
3 g +216.1 g - 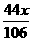
x = 10.6 g
-------------------------------------- -------------------------------1分
-------------------------------1分
HCl的质量=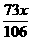 =
=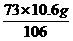 =7.3g
=7.3g
稀盐酸的质量分数=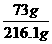 ×100%=3.4%--------------------------------1分
×100%=3.4%--------------------------------1分
答:稀盐酸的质量分数为3.4%。
35. (3分)解:设固体混合物中碳酸钠的质量为x
Na2CO3+2HCl 2NaCl+ CO2↑+H2O …………………………1分
106 73 117 44
x 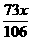
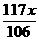
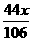
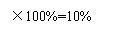 (22.3-x) g
+
(22.3-x) g
+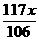
34.(3分)解:设至少需要参加反应的氧化铝的质量为x
|
Al2O3+N2+3C 2AlN+3CO
 10
10 2 82
2 82
x 41Kg …………………………1分
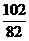 =
=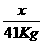 或
或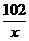 =
=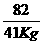 …………………………1分
…………………………1分
x =102×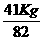 =51Kg …………………………1分
=51Kg …………………………1分
答:至少需要参加反应的氧化铝的质量为51Kg。
33.(8分,每空l分。)
[实验探究] 稀盐酸、硫酸铜等;冒气泡、出现红色固体等
[理论探讨] l535℃-l538℃ Fe2O3 Fe3O4
[拓展延伸](1) 在集气瓶底部放少量的水(或在集气瓶底部铺一层细沙) (2) 由黑色变成红棕色
(3) A>C>B
|
(1)2H2O2 2H2O + O2↑ 催化
(2)CaCO3+2HCl CaCl2 + H2O+CO2↑  ⑦
⑦
(3)A D或E或F
32.(5分,每空l分。)
|
现象,并写出 C中发生反应的化学方程式 |
B中有气泡产生,C中澄清石灰水变浑浊
Ca(OH)2+CO2 CaCO3↓+ H2O  |
|
上述现象产生的原因 |
B中不断产生
 CO2,压强增大,将B中碳酸钠溶液压入A中,和A中的澄清石灰水发生反应,生成碳酸钙白色沉淀 CO2,压强增大,将B中碳酸钠溶液压入A中,和A中的澄清石灰水发生反应,生成碳酸钙白色沉淀
|
|
现象 |
紫色石蕊变红
|
|
写出A中X溶液的溶质 |
Na2CO3、
NaHCO3 (K2CO3)
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com