
题目列表(包括答案和解析)
18.在密闭容器中给CO和水蒸气的混合物加热到800℃时,有下列平衡:

 ;且K=1,若用2 mol CO和
;且K=1,若用2 mol CO和 (气)相互混合并加热到800℃,则CO的转化率为:
(气)相互混合并加热到800℃,则CO的转化率为:
A.16.7% B.50% C.66.7% D.83.3%
17.下图各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是 ( )
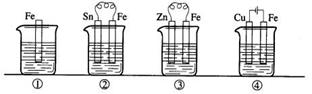 A.④>②>①>③
A.④>②>①>③
B.②>①>③>④
C.④>②>③>①
D.③>②>④>①
16.在容积固定的密闭容器中存在如下反应:
A(g)+3B(g) 2C(g);△H<0
2C(g);△H<0
 某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出上述关系图:下列判断一定错误的是
某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出上述关系图:下列判断一定错误的是
A.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高
C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
15.某温度下,有两瓶不同浓度的氨水,甲瓶的浓度为0.1mol/L ,乙瓶的浓度为1mol/L,则甲瓶溶液中[OH-]与乙瓶之比为 ( )
A.= 1/10 B大于1/10 C小于1/10 D.无法确定
14.水是一种极弱电解质,在室温下平均每n个水分子中只有一个水分子发生电离,则n值为
A. 1×10-14 B. 55.6×107 C. 107 D. 55.6
13.关于可逆反应C(s)+ CO2(g)
 2C0(g);△H > 0 平衡常数为K,下列说法错误的是
2C0(g);△H > 0 平衡常数为K,下列说法错误的是
A. k = 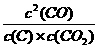

B. K值越大表示达到平衡时,正反应进行程度越大
C.其它条件不变时,温度改变,K值改变
D.其它条件不变时,压强改变,K值不改变
12.在由水电离产生的c(H+)=1×10-14mol/L的溶液中,一定可以大量共存的离子组是
A. H+.Al3+.Br-.SO42- B. Na+.Mg2+.Cl-.NO3-
C. K+.Ba2+.Cl-.NO3- D. K+.Na+.SO32-.SO42-
11.25℃时,水的电离达到平衡:H2O H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是
A. 向水中加入稀氨水,平衡逆向移动,c(OH―)降低
B. 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C. 向水中加入少量固体CH3COOH,平衡逆向移动,c(H+)降低
D. 将水加热,Kw增大,pH不变
10.某反应过程中体系的能量变化如图所示,下列说法错误的是 ( )
 A.反应过程可表示为
A.反应过程可表示为
A+BC-→[A…B…C] -→AB+C
(反应物)(过渡态) (产物)
B.E1为反应物的平均能量与过渡态的能量差,称 为正反应的活化能
C.正反应的热效应为△H=E1-E2,且E2>E1,所以正反应为放热反应
D.此图中逆反应的热效应△H=E1-E2,为吸热反应
9.在373K时,把0.5molN2O4气通入体积为5L 的真空密闭容器中,立即出现棕色.反应进行到2s时,NO2的浓度为0.02mol/L.在60s时,体系已达平衡,此时容器内压强为开始时的1.6倍.下列说法正确的是
A.前2s,以N2O4的浓度变化表示的平均反应速度为0.01mol/(L•s)
B.在2s时体系内的压强为开始时的1.1倍
C.在平衡时体系内含N2O40.25mol
D.平衡时,如果压缩容器体积,则可提高N2O4的转化率
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com