
题目列表(包括答案和解析)
6、化学学习让我们转变了生活态度和观念,形成了更加科学的生活方式。下列有关说法中不正确的是
A.洗涤剂具有乳化功能,可以去除餐具上的油污
B.食用适量富含维生素A的动物肝脏可预防夜盲症
C.常食新鲜蔬菜、水果,可获得丰富的维生素C
D.电木插座开裂后,可用加热熔化的方法修补
|
实验内容 |
实验现象 |
|
①+② |
有白色沉淀生成 |
|
②+④ |
有白色沉淀生成 |
|
①+③ |
有气泡冒出 |
5、英国科技人员研制出自动灭火陶瓷砖,砖里压入了一定量的氦气和二氧化碳。这种砖砌成的房屋发生火灾时,在高温烘烧下,砖会裂开并喷出氦气和二氧化碳,从而抑制和扑灭火焰。自动灭火陶瓷砖的灭火原理是
A.清除可燃物 B.使燃烧物与氧气隔绝
C.降低燃烧物的着火点 D.使燃烧物的温度降低到着火点以下
4、硒是人体必需的一种微量元素,严重缺硒有可能诱发皮肤疾病。已知硒的原子序数为34,质子数与中子数之和为79。下列有关硒原子的说法中,不正确的是
A.核外电子数为34 B.核电荷数为79
C.质子数为34 D.中子数为45
3、在一定环境中,常温常压下的水可以瞬间结成冰,俗称”热冰”。下列说法正确的
A.”热冰”是纯净物 B.“热冰”在任何条件下都不会熔化
C.“热冰”与水的化学性质不同 D.结成“热冰”后,分子停止运动
2、搜救人员克服严重的高原反应等困难,全力展开搜救。吸氧是克服高原反应的方法之一,吸氧可以帮助搜救人员的高原反应的原因是
A. 氧气可供呼吸 B. 氧气可以燃烧
C.氧气可以支持燃烧 D.氧气是无色无味的无毒气体
1、下列常见物质的用途,主要利用其物理性质的是

A.压缩天然气做燃料 B.金属铜用于制导线 C.氮气用于食品防腐 D.石灰中和酸性土壤
2、步骤②通入氮气的目的是: ▲
[实验结论]
该绿色粉末的组成元素是: ▲ ;各元素的质量比为: ▲ (写出计算过程)
1、老师看了实验方案后认为,从环保的角度来看,此装置有一个缺陷,建议装置D后还应添加一个酒精灯,并在实验步骤 ▲ (填实验步骤的序号)中点燃
28.聪聪同学在实验室帮老师整理废弃药品时发现一瓶没有标签的绿色粉末,对其组成很好奇。征得老师允许后,设计了以下实验进行探究。
|
操作步骤 |
实验现象 |
结论或化学反应方程式 |
|
取少量样品置于试管中,加入足量稀硫酸,将试管用导管与澄清石灰水相连。 |
①产生大量气体,使石灰水变浑浊。 ②样品全部溶解,溶液呈蓝色。 |
①样品中含有 ▲ 离子 ②样品中含有 ▲ 离子 |
|
在上述蓝色溶液中,插入一根洁净的铁丝。 |
①铁丝表面缓缓产生少量气泡。 ②片刻后铁丝表面出现红色物质。 |
① ▲
② ▲ (均用方程式表示) |
为了进一步确定该物质的元素组成,查阅部分资料后,他继续进行了实验。
[资料查阅]白色的无水硫酸铜可做吸水剂,遇水会变成蓝色。
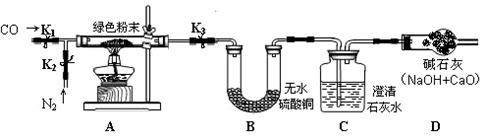 [实验步骤]
[实验步骤]
①如图搭建实验仪器,并检验装置的气密性。
②在A装置中装入11.1g绿色粉末。关闭K1,打开K2、K3,持续通入适量N2。
③关闭K2、K3,分别称量装置B、C、D的质量,记录数据。
④打开K3,点燃酒精灯加热绿色粉末直至装置C中无气泡产生时,关闭K3,熄灭酒精灯。分别称量装置B、C、D的质量,记录数据。
⑤待A冷却后,打开K1、K3,持续通入适量CO,再次点燃酒精灯加热。
⑥当A中粉末全部变红后,熄灭酒精灯。试管冷却后,关闭K1。称量装置A、B、C、D的质量,记录数据。
[实验现象和数据处理]
|
|
装置A |
装置B |
装置C |
装置D |
|
第一次 加热后 |
绿色粉末变黑色 |
▲ 质量增加0.9g |
出现白色沉淀, 质量增加2.2g |
无明显变化 质量不改变 |
|
第二次 加热后 |
黑色粉末变红色 质量为6.4g |
无明显变化, 质量不改变 |
沉淀先增加后部分溶解; 质量增加 |
无明显变化 质量不改变 |
[实验分析与反思]
27.(7分)实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数。
(1)配制200g质量分数为4%的氢氧化钠溶液,需要氢氧化钠固体的质量为 ▲ g,水的体积为 ▲ mL(水的密度近似看作1g/cm3)。
 (2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为
(2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为
4%的氢氧化钠溶液,用pH计(一种测定溶液pH的仪器)
测定溶液的pH,得到的数据如下:
|
加入氢氧化钠 的体积/mL |
0 |
1.0 |
8.0 |
9.5 |
10.5 |
12.0 |
16.5 |
|
烧杯中溶液pH |
1.0 |
1.3 |
2.0 |
3.9 |
9.9 |
11.9 |
12.8 |
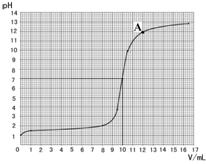
依据表中数据绘制出烧杯中溶液的pH与加入氢氧
化钠溶液体积(V)之间的变化关系图。
(3)根据上图查出氢氧化钠与盐酸恰好完全反应时,所滴加氢氧化钠溶液的体积为 ▲ mL,A点所表示的溶液中溶质的化学式为 ▲ 。
(4)计算此瓶盐酸的溶质质量分数。(请写出计算过程。氢氧化钠溶液的密度按1.0g/mL计算) ▲
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com