
题目列表(包括答案和解析)
7.反应4NH3(g)+5O2(g)==4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45
mol,则此反应的平均速率 (X)(反应物的消耗速率或产物的生成速率)可表示为
(X)(反应物的消耗速率或产物的生成速率)可表示为
A. (NH3)=0.010 mol·L-1·s-1
B.
(NH3)=0.010 mol·L-1·s-1
B. (O2)=0.0010 mol·L-1·s-1
(O2)=0.0010 mol·L-1·s-1
C. (NO)=0.0010 mol·L-1·s-1 D.
(NO)=0.0010 mol·L-1·s-1 D. (H2O)=0.045 mol·L-1·s-1
(H2O)=0.045 mol·L-1·s-1
6.决定化学反应速率的主要原因是
A.参加反应物质的性质 B.加入催化剂
C.温度和压强 D.各反应物和生成物的浓度
5.下面是中学阶段某些同学在实验操作中记录下的实验数据,其中错误的是
A.用托盘天平称取29.3g食盐晶体
B.用广泛pH试纸测某碱性溶液,试纸由白色变为蓝黑色,pH为10.5
C.用标准盐酸滴定未知苛性钠溶液时用去酸液9.98mL
D.用10mL量筒量取4.3mL浓硫酸溶液
4.物质的水溶液能导电,且该物质属于非电解质,溶于水时化学键被破坏的是
A.氯化氢 B.蔗糖 C.干冰 D.硫酸钡
3.常温下,在pH=11的某溶液中,由水电离出的c (OH- )可能为
①1.0×10-3 mol/L ②1.0×10-6 mol/L
③1.0×10-7 mol/L ④1.0×10-11 mol/L
A.①③ B.③ C.④ D.①④
2.一定条件下,对于可逆反应2HBr(g) H2(g)+Br2(g),下列叙述能够说明反应达到平衡状态的是
H2(g)+Br2(g),下列叙述能够说明反应达到平衡状态的是
A.压强保持不变 B.断裂2mol H-Br键的同时生成1mol H-H键
C.混合气体的平均式量不变 D.混合气体颜色不再发生变化
1.“84”消毒液在疾病预防中被广泛使用。该消毒液无色,pH大于7,对某些有色物质有漂白作用。你认为它可能的有效成分是
A.SO2 B. Na2CO3 C.KMnO4 D.NaClO
23、(8分)(1)已知1molCO气体完全燃烧生成CO2气体放出283kJ的热量; 1molH2完全燃烧生成液态水放出286kJ热量;1molCH4气体完全燃烧生成CO2气体和液态水放出890kJ热量。
①写出CH4燃烧的热化学方程式 。
②若1molCH4气体完全燃烧生成CO2气体和水蒸气,放出的热量 (填>、<、=) 890kJ。
③若将amol CH4、CO 、H2的混合气体完全燃烧,生成CO2气体和液态水时,则放出的热量(Q)的取值范围是 。
(2)已知下列热化学方程式:
①Fe2O3(s)+3CO(g)=Fe(s)+3CO2 (g) △H=-25kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+ CO2(g) △H=+19kJ/mol
写出FeO(s)被CO还原成Fe和CO2的热化学方程式 。
22、(10分)某工厂的废液经测定含有甲醇、乙醇、乙酸和乙酸乙酯,欲从废液中回收乙醇和乙酸,重新加以利用。有关数据,实验仪器和试剂如下:
|
|
甲醇 |
乙醇 |
乙酸 |
乙酸乙酯 |
乙酸钠 |
|
m.p.(OC) |
-97.8 |
-117.3 |
16.6 |
-83.6 |
324 |
|
b.p. (OC) |
65.7 |
78.4 |
118 |
77.1 |
|
250mL蒸馏烧瓶;400mL烧杯;250mL烧杯;冷凝管;温度计;玻璃棒;酒精灯和其他夹持仪器。1mol/LNaOH溶液;18.4mol/LH2SO4溶液。
(1) 填写下列实验步骤中的空白。
①组装蒸馏装置,检查器其气密性。
②温度计插入蒸馏烧瓶的 (填选项序号)
a.烧瓶口 b.支管口处 c.蒸馏液中
冷凝管冷却水的流向 (填选项序号)
a.下口进水,上口出水 b. 上口进水,下口出水
③取100mL废液加入250mL蒸馏烧瓶中,加入碎瓷片,滴入1mol/LNaOH溶液,调节pH=10。
④将接收器置于冷凝管下,缓慢加热蒸馏烧瓶,待温度升至78.4OC得到乙醇。
⑤ ,得到乙酸。
(2)蒸馏前,在烧瓶中加入1mol/LNaOH溶液,调节pH=10的作用是 ,
(3)若想得到纯净的乙醇溶液,且不污染环境,在得到乙醇前,尚需补充的操作是
。
21、(10分)已知(1)通常Br2与C=C键起加成反应,但高温下Br2易取代与C=C键直接相连α-碳原子上的氢原子: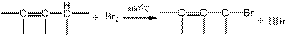
(2)与苯环直接相连的支链碳原子上的氢原子也易被溴取代:

根据上述信息,结合所学知识,设计一个以丙苯为原料合成1-苯丙三醇(C6H5CHOHCHOHCH2OH)的方案(用合成路线流程图表示,并注明反应条件)。合成路线流程图示例如下:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com