
题目列表(包括答案和解析)
4.下列对一些事实的解释不正确的是
|
|
事 实 |
解 释 |
|
A |
物质的热胀冷缩 |
分子或原子间的间隔随温度的改变而改变。 |
|
B |
一氧化碳有可燃性,而二氧化碳不具有可燃性 |
物质组成元素不同,分子结构也不同 |
|
C |
0℃时水结成冰,而海水在-1.9℃才会结冰 |
海水中含有盐,是混合物,其凝固点比水低 |
|
D |
溶液之间的化学反应比固体之间的化学反应快 |
参加反应的粒子在溶液中接触的机会比在固体中接触的机会多 |
3.某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水蒸气都是可再生能源;③使用车用乙醇汽油防止“温室效应;④不锈钢和目前流通的硬币都是合金;⑤推广使用无氟冰箱防止“臭氧空洞”;⑥纯碱和熟石灰都是碱。其中说法完全正确的组合是
A. ①③④⑤ B.①②⑤⑥ C.③⑤⑥⑦ D.①④⑤
2.如下图所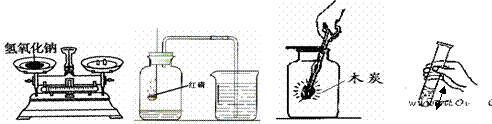 示,实验装置或实验基本操作中,正确的是
示,实验装置或实验基本操作中,正确的是

A B C D
1.下列变化中,只发生了物理变化的是
A.汽油挥发 B.白磷自燃 C.燃放烟花 D.高炉炼铁
28.作为推行“低碳经济”的重要科技进步,太阳能光伏发电成为2010年上海世博会的“亮点”。太阳能光伏发电最关键的材料是高纯硅,三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法.生产流程示意如下:

(1)石英砂的主要成分是SiO2,工业上制取粗硅的化学方程式为:SiO2
+ 2C  Si + 2R,R的化学式为
;该反应的基本类型是
。
Si + 2R,R的化学式为
;该反应的基本类型是
。
(2)整个制备过程必须达到无水无氧。在H2还原SiHCl3过程中若混入O2 ,可能引起的后果是 。
(3)为了达到绿色化学和资源综合利用的目的,在生产过程中物质A需要循环使用,A的化学式是 。
27.草酸(H2C2O4)是一种二元酸,在一定条件下受热会发生分解,某实验小组对草酸分解产物的可能组合进行了多种假设:①H2、CO;②H2、CO2;③H2O、CO;④H2O、CO2;⑤H2O、CO、CO2。
(1)在这些假设中,可以运用初中化学所学的相关知识并通过一定的逻辑推理直接排除的是___________________(填编号),其它的则需要通过实验进行验证。
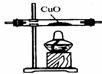
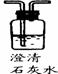
(2)如下图,实验室提供下列盛有药品的仪器,验证草酸分解的可能产物。
 |
 |
 |
 |
|
A |
B |
C |
D |
① 证明其中含有水蒸气,出现的实验现象是 。
② 证明其中含有二氧化碳,反应的化学方程式是 。
③ 用上述仪器(可以重复使用)组装一套装置,通过一次实验验证草酸分解的可能产物,按气体通过的先后顺序,连接的仪器依次是 (用A、B、C、D表示)。
④从环境保护角度出发,该实验中最后导出的尾气的处理方法是____________ 。
26.实验室用加热固体氯化铵和熟石灰制取氨气(2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O)。
CaCl2+2NH3↑+2H2O)。
(1)写出下列实验装置中标号a、b的仪器名称:a 、b 。
(2)实验室制取氨气应选用的发生装置是 (填以下标号);其收集装置可选用E,但最好选用F,且进气口是e,其可能的原因是 。
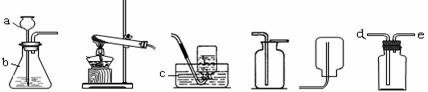

A B C D E F G
(3)请根据化学方程式列式计算,制取0.6mol氨气,至少需要熟石灰多少摩尔?
25. 某同学在自主学习金属的知识时,设计以下实验报告,请将该实验报告补充完整。
[实验目的] 。
[实验用品]铁片、铜片、镁片、稀盐酸、硫酸铜溶液、硝酸银溶液
[实验内容]
|
实验步骤 |
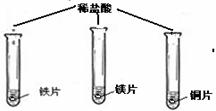 (在同温下,取大小相同、光亮的三种金属薄片,投入等体积、等浓度的足量稀盐酸中) (在同温下,取大小相同、光亮的三种金属薄片,投入等体积、等浓度的足量稀盐酸中) |
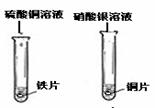 |
|
实验现象 |
铁片和镁带表面都有气泡产生, 铜片表面却没有明显现象。 |
铁片表面有
,铜片表面有银白色固体析出。 |
|
分析 结论 |
铁与稀盐酸反应的化学方程式: , 活泼金属能与酸(稀盐酸)反应。 |
铁与硫酸铜溶液反应的化学方程式:
, 某些金属能与盐溶液发生反应 。 |
[实验思考]通过上述实验,能否证明Fe、Cu、Ag三种金属的活动性顺序?并说明理由:
。
24.固体A中可能含有Na2SO4、FeCl3、Na2CO3、KCl中的一种或几种, 进行如下实验,观察、记录现象,并逐步推出结论。请完成下表:
|
实验步骤及现象 |
结论 |
|
①将少许A溶于水得到无色溶液B。 |
A中一定没有 |
|
②在B中加入足量BaCl2溶液,生成白色沉淀C,过滤得滤液D。 |
A中一定有 |
|
③在C中加入足量稀硝酸,C部分溶解;在D中加入AgNO3溶液,生成的白色沉淀不溶于稀硝酸。 |
|
|
④另取少许A进行焰色反应,透过蓝色钴玻璃片,观察到火焰呈 色。 |
A中还有KCl |
23.将一定溶质质量分数的浓盐酸盛于烧杯中,敞口放置在实验室安全之处。
 (1)浓盐酸的溶质质量分数和放置天数关系的曲线(见右图)正确的是 (填写“甲”或“乙”)。
(1)浓盐酸的溶质质量分数和放置天数关系的曲线(见右图)正确的是 (填写“甲”或“乙”)。
(2)随着放置天数的增加,浓盐酸的溶质质量分数发生变化的主要原因是 。
(3)把浓盐酸稀释后可用于去除铁制品表面的铁锈(主要成分为 Fe2O3),
反应的化学方程式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com