
题目列表(包括答案和解析)
6、铅蓄电池总反应为:Pb + PbO2+2H2SO4 2PbSO4+2H2O,下列关于铅蓄电池的说法正确的是
2PbSO4+2H2O,下列关于铅蓄电池的说法正确的是
A.在放电时,正极发生的反应是 Pb(s) +SO42-(aq) → PbSO4(s) +2e-
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是PbSO4(s)+2e-→ Pb(s)+ SO42-(aq)
5、下列说法或表示方法正确的是
A.若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由“C(石墨)=C(金刚石) ΔH=1.9kJ·mol-1”可知,金刚石比石墨稳定
C.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=285.8 kJ·mol-1
D.CaCO3(s)=CaO(s)+CO2(g) △H>0,△S>0,则:该反应在高温下能自发进行
4、某学生的实验报告所列出的下列数据中合理的是( )
A.用10mL量筒量取7.13mL稀盐酸
B.用托盘天平称量25.20g NaCl
C.用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL
3、下列关于铜电极的叙述中正确的是
A.铜锌原电池中铜是负极
B.用电解法精炼粗铜时粗铜作阳极
C.在铁上电镀铜时用铜作阴极
D.电解稀硫酸时用铜作阳极,阳极产生氧气
2、在0.1 mol·L-1 CH3COOH溶液中存在如下电离平衡CH3COOH CH3COO-+H+ 对于该平衡,下列叙述正确的是( )
CH3COO-+H+ 对于该平衡,下列叙述正确的是( )
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
1、勤洗手和经常对环境进行消毒是预防传染病的有效途径。某消毒液为无色液体,用红色石蕊试纸检验,发现试纸先变蓝后褪色。则该消毒液的主要成分可能是
A.KMnO4 B.H2O2 C.NaClO D.NH3·H2O
26. 某化学兴趣小组在实验失室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。
②氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:
3Cl2+6OH- 5Cl-+ClO3-+3H2O
5Cl-+ClO3-+3H2O
该兴趣小组设计了下列实验装置,进行实验。

请回答下列问题:
(1)①甲装置用于制备氯气,乙装置的作用是____________。
②该兴趣小组用100mL 12mol/L盐酸与8.7g MnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2______________g。
 (2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。他们讨论后认为,部分氯气未与石灰乳反应而逸出,以及温度升高是可能原因。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢。匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为右图(不考虑氯气和水的反应)。
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。他们讨论后认为,部分氯气未与石灰乳反应而逸出,以及温度升高是可能原因。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢。匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为右图(不考虑氯气和水的反应)。
①图中曲线I表示_____________离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为______________mol。
③另取一份与②等物质的量的石灰乳,以较大的速率通入足量氯气,反应后测得产物中 的物质的量为0.37mol,则产物中
的物质的量为0.37mol,则产物中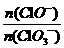 =______________。
=______________。
(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进。请你给出一种改进方法:_____________。
25. 下图是一些常见的单质.化合物之间的转化关系图,有些反应中的部分物质被略去。常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质。反应①②均为工业上的重要反应。

请回答下列问题:
(1)D的电子式为_______________。
(2)K的化学式为_______________。
(3)写出B与C高温反应生成E和F的化学方程式:______________。
(4)写出D与J的稀溶液反应生成G的离子方程式:______________。
24.(15分)本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分.
A.《化学与生活》。
(1) 合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①维生素C能增强人体对疾病的抵抗能力,促进人体生长发育,中学生每天要补充60mg的维生素C。下列物质含有丰富维生素C的是 (填字母)。
A.牛肉 B.辣椒 C.鸡蛋
②青少年及成人缺乏某种微量元素将导致甲状腺肿大,而且会造成智力损害,该微量元素是
( 填字母)
A.碘 B.铁 C.钙
③蛋白质是人体必需的营养物质,它在人体内最终分解为 (填字母)。
A.葡萄糖 B.氨基酸 C.脂肪酸
(2) 材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是 。
②玻璃是重要的硅酸盐产品。生产玻璃时,石灰石与石英反应的化学方程式为 。
③铁是人们生活中常用的金属材料,请列举两种防止铁制品被腐蚀的方法:
. 。
(3) 保持洁净安全的生存环境已成为全人类的共识,人与自然要和谐相处。
①pH< 的雨水称为酸雨;向煤中加入适量的 ,可以大大减少燃物产物中SO2的量。
②对汽车加装尾气催化净化装置,可以使其中的NO、CO相互反应转化成无毒的气体,其原理可以用化学方程式表示为 。
③天然水中杂质较多,常需加入明矾,ClO2等物质处理后才能饮用。加入ClO2的作用是 ;加入明矾后,Al3+水解的离子方程式是 。
B.《有机化学基础》
(1) 具有明显现象的官能团特征反应常被用来鉴定化合物。
①欲区分CH3 CH2OH和CH3 CHO,应选用 (填字母)。
A.NaOH溶液 B.银氨溶液 C.盐酸
②欲区分 和
和 ,应选用
(填字母)。
,应选用
(填字母)。
a.KMnO4溶液 b.溴水 c.Na2CO3溶液
③欲区分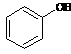 和
和 ,应选用
(填字母)。
,应选用
(填字母)。
a.AgNO3溶液 b.NaOH溶液 c.FeCl3溶液
(2) 在有机化学中,同分异构是普遍存在现象。分子式为C4H9Br的有机物共有 种。其中,一种有机物通过消去反应可转变为2-丁烯,请写出该消去反应的化学方程式 ;另一种有机物的核磁共振氢谱图(1H核磁共振谱图)中显示一个峰,请写出该有机物的结构简式如下: 。
(3) 聚丁二酸乙二醇酯(PES)是一种生物可降解的聚酯,它在塑料薄膜,食品包装和生物材料方面有着广泛的应用。其结构简式如下:

①聚丁二酸乙二醇酯(PES)是由两种单体通过 反应(填反应类型)制得的。形成该聚合物的两种单体是 和 。
②这两种单体相互之间也可能形成一种八元环状酯,请写出该环状化合物的结构简式: 。
23. 某溶液中可能含有下列6种离子中的某几种:Cl-、SO42-、CO32-、NH4+、Na+、K+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是 ( )
A.一定存在SO42-、CO32-、NH4+,可能存在Cl-、Na+、K+
B.一定存在SO42-、CO32-、NH4+、Cl-,一定不存在Na+、K+
C.c(CO32-)=0.01mol·L-1,c(NH4+)>c(SO42-)
D.如果上述6种离子都存在,则c(Cl-)>c(SO42-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com