
题目列表(包括答案和解析)
4. 可以判断油脂皂化反应基本完成的现象是( )
A.反应液使红色石蕊试纸变蓝色
B.反应液使蓝色石蕊试纸变红色
C.反应后静置,反应液分为两层
D. 反应后静置,反应液不分层
3.下列关于常见有机物的说法不正确的是 ( )
A. 乙烯和苯都能与溴水反应
B. 乙酸和油脂都能与氢氧化钠溶液反应
C. 糖类和蛋白质都是人体重要的营养物质
D. 乙烯和甲烷可用酸性高锰酸钾溶液鉴别
2.下列关于有机物的说法错误的是 ( )
A.CCl4可由CH4制得,可萃取碘水中的碘
B.石油和天然气的主要成分都是碳氢化合物
C.乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别
D.苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应
1.下列涉及有机物的性质或应用的说法不正确的是 ( )
A.淀粉、纤维素、蛋白质都是天然高分子化合物
B.用于奥运“祥云”火炬的丙烷是一种清洁燃料
C.用大米酿的酒在一定条件下密封保存,时间越长越香醇
D.纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应
3.Ⅱ卷卷头和答题卡均填涂本次考试的考号,不要误填学号。
相对原子质量:H=1;C=12;N=14;O=16;Na=23; Al=27;S=32;Cl=35.5;
卷Ⅰ(选择题 共57分)
选择题(本题包括22小题,1-15题每小题2分,16-24每小题3分,共计57分。在每小题给出的四个选项中,只有一个选项符合题意。)
2.将卷Ⅰ答案用2B铅笔涂在答题卡上,卷Ⅱ用蓝黑钢笔或圆珠笔答在试卷上。
26.N2和H2发生合成氨反应N2(g)+3H2(g) 2NH3(g)。在一定条件下达到平衡时,各物质的浓度是c(N2)=3mol/L,c(H2)=9mol/L,c(NH3)=4mol/L,求该温度时的平衡常数及N2、H2的起始浓度。
2NH3(g)。在一定条件下达到平衡时,各物质的浓度是c(N2)=3mol/L,c(H2)=9mol/L,c(NH3)=4mol/L,求该温度时的平衡常数及N2、H2的起始浓度。
 2010/2011学年度第二学期期中考试试卷
2010/2011学年度第二学期期中考试试卷
25.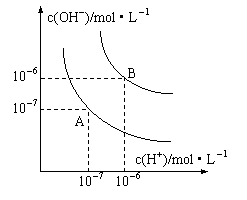 (8分)水的电离平衡曲线如右图所示。
(8分)水的电离平衡曲线如右图所示。
(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从 增加到 。
(2)将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持100℃的恒温,欲使混合溶液pH=7,则Ba(OH)2溶液与盐酸的体积比为 。
(3)已知AnBm的离子积=[c(Am+)]n·[c(Bn-)]m,式中c(Am+)n和c(Bn-)m表示离子的物质的量浓度。在某温度下,Ca(OH)2的溶解度为0.74g,其饱和溶液密度设为1g/mL,其离子积为 。(原子量Ca:40,O:16,H:1)
24.(12分)在800℃时,2L密闭容器内,2NO(g)+O2(g) 2NO2(g)反应体系中,n(NO)随时间的变化如表:
2NO2(g)反应体系中,n(NO)随时间的变化如表:
|
时间/s |
0 |
1 |
2 |
3 |
4 |
|
n(NO)/mol |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
(1)写出该反应的平衡常数表达式:K= 。
 已知:
已知: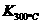 >
>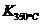 ,则该反应是 热反应。
,则该反应是 热反应。
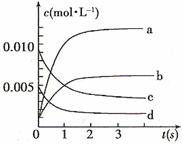
(2)右图中表示NO2的变化的曲线是 ;
用O2表示从0-2 s内该反应的平均速率v= 。
(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
23.(4分)已知下列反应的反应热:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H=-870.3kJ∕mol
②C(S)+O2(g)=CO2(g) △H=-393.5kJ∕mol
③2C(S)+2H2(g)+O2(g)=CH3COOH(l) △H=-488.3kJ∕mol
请写出H2燃烧热的热化学方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com