
题目列表(包括答案和解析)
10.NaF、NaI、MgO均为离子化合物,由下列表中数据可确定这三种化合物熔点高低的顺序,则正确的是( )
|
物质 |
①NaF |
②NaI |
③MgO |
|
离子电荷数 |
1 |
1 |
2 |
|
键长/10-10m |
2.31 |
3.18 |
2.10 |
A.① > ② > ③ B.③ > ① > ② C.③ > ② > ① D.② > ① > ③
9.已知三角锥形分子E和直线形分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10)如下图,则下列判断错误的是( )
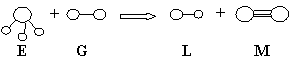

A.G是最活泼的非金属单质 B.L的稳定性小于E
C.E能使紫色石蕊试液变蓝色 D.M化学性质比较稳定
8.下列说法中正确的是 ( )
A.NO2、SO2、BF3分子中所有原子的最外层电子都满足了8e-稳定结构 B.P4和CH4都是正四面体分子且键角都为109o28ˊ C.NaCl晶体中与每个Na+距离相等且最近的Na+共有12个 D.原子间通过共价键而形成的晶体一定具有高的熔、沸点及硬度
7. X、Y两元素的质子数之和为22,X的原子核外电子数比Y少6个,下列说法中不正确的是( )
A.Y的单质是原子晶体 B.X的单质固态时为分子晶体
C. X与碳形成的化合物为分子晶体 D. X与Y形成的化合物固态时为离子晶体
6. 下列物质性质的变化规律与分子间作用力有关的是 ( )
A.HF、HCl、HBr、HI的热稳定性依次减弱 B.金刚石的硬度大于硅,其熔、沸点也高于硅
C.NaF、NaCl、NaBr、NaI的熔点依次降低 D.F2、Cl2、Br2、I2的熔、沸点逐渐升高
5.共价键、离子键、金属键、范德华力和氢键都是微观粒子之间的不同作用力,下列物质:①Na2O2;②冰;③金刚石;④碘单质;⑤CaCl2;⑥白磷,其中只含有两种作用力的组合是 ( )
A.①④⑥ B.①③⑥ C.②④⑥ D.①②③⑥
4.下列关于丙烯(CH3-CH =CH2)的说法正确的( )
A. 丙烯分子有7个δ键,1个π键 B. 丙烯分子中3个碳原子都是sp3杂化。
C. 丙烯分子存在非极性键。 D. 丙烯分子中3个碳原子在同一直线上。
3.下列各组物质发生状态变化时,所克服的微粒间的相互作用,属于同种类型的是 ( )
A.钠和硫的熔化 B.食盐和石蜡的熔化
C.碘和干冰的升华 D.二氧化硅和氧化钠的熔化
2.现有四种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4; ②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是
A.第一电离能:③>②>① B.原子半径:③>②>①
C.电负性:③>②>① D.最高正化合价:③>②>①
1.下列各组物质中,按熔点由低到高排列,正确的是( )
A、O2 、I2 、Hg B、CO2 、KCl 、SiO2 C、Na 、K 、Rb D、SiC 、NaCl 、SO2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com