
题目列表(包括答案和解析)
1. 下列有关化学用语使用正确的是( )
A. 硫原子的原子结构示意图为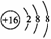 B.
NH4Cl的电子式为:
B.
NH4Cl的电子式为: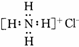
C.原子核内有10个中子的氧原子: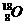 D.
对氯甲苯的结构简式为:
D.
对氯甲苯的结构简式为:
22. (12分)请回答氯碱的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比例k(质量比)生成的产品。理论上k=__________(要求写出计算表达式和结果)。
(2)原料粗盐中常含有泥沙和Ca2+,Mg2+,Fe3+,SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水中过滤后,还要加入的试剂分别为①Na2CO3,②HCl(盐酸),③BaCl2,这3种试剂添加的合理顺序是____________(填序号)。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中X,Y分别是________,_________(填化学式),分析并比较图中氢氧化钠质量分数a%与b%的大小_____________。
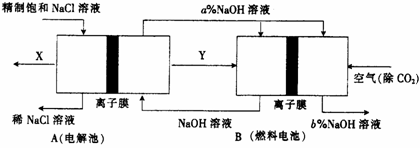
②分别写出燃料电池B中正极、负极上发生的电极反应。正极:___________________。
负极:___________________________。
③这样设计的主要节(电)能之处在于(写出2处): 、 .
21. (8分)从铝土矿(主要成分是Al2O3,含SiO2,Fe2O3,MgO等杂质)中提取两种工艺品的流程如下图所示:

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的方程式为_________________.
(2)流程乙加入烧碱后生成SiO32-的离子方程式为______________.
(3)验证滤液B含Fe3+,可取少量滤液并加入____________(填试剂名称)。
(4)滤液E,K中溶质的主要成分是___________(填化学式),写出该溶液的一种用途_____________.
(5)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的滤液B,加入一定量的烧碱达到沉淀溶液平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=__________.
20. (10分)化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体。可由马铃薯、玉米、淀粉等发酵制得。A的钙盐是人们喜爱的补钙剂之一,A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应,在浓硫酸存在下,A可发生如图所示的反应:
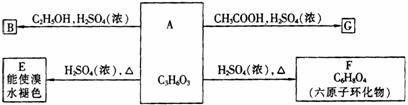
(1)写出化合物A,B,G的结构简式:A_________,B________,G__________。
(2)写出有关化学方程式。
A→E ;
A→F ;
(3)写出反应类型:A→E__________,A→F____________.
(4)与A具有相同官能团的同分异构体的结构简式为 .
19. (6分)用一种试剂将下列各组物质鉴别开.
(1) 和
和 :
:
(2)  ,
, 和C6H12(已烯):
和C6H12(已烯):
(3)  ,CCl4和乙醇 .
,CCl4和乙醇 .
18. (8分)Ⅰ. 有机物的结构可用“键线式”简化表示。CH3-CH=CH-CH3可简写为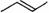
有机物X的键线式为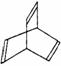
(1)有机物Y是X的同分异构体,且属于芳香烃,请写出Y的结构简式: 。
(2)Y与乙烯在一定条件下发生等物质的量聚合反应,请写出其反应的化学方程式;___________________。
(3)X与足量的H2在一定条件下反应可生成环状和烃Z,Z的一氯代物有_________种。
Ⅱ. 1991年诺贝尔化学奖授予瑞士化学家R.R.Ernst教授,以表彰他在发展高分辨核磁共振波谱学方面的杰出贡献。1H核磁共振谱(PMR)是研究有机化学分子结构的一种重要方法。已知有机化合物中处于同一位置的氢原子(称为等性氢原子)在PMR中为同一组信号峰,谱中峰的强度与分子中给定类型的氢原子数成正比。例如CH2=CHCH2CH3有四种不同位置的氢原子,因此在PMR中有4组信号峰,强度比为2:1:2:3
(1)乙醇(CH3CH2OH)在PMR中可能有_______组信号峰,甲醚(CH3OCH3)在PMR中可能有______组信号峰。
(2)在常温下测得某烃C8H10的PMR谱,观察到两种氢原子给出的信号,其强度之比为2:3,该烃的结构简式可能为_________。
17. (8分)在下列物质中:
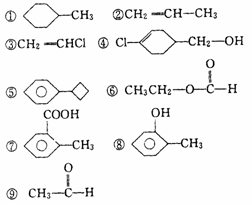
属于脂肪烃的是_________,属于芳香化合物的是__________,属于卤代烃的是___________,属于醇的是_________,属于酚的是__________,属于醛的是___________,属于酸的是_____________,属于酯的是____________。
16. 海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是( )
A. 海水中含有钾元素,只需经过物理变化就可以得到钾单质
B. 海水蒸发制海盐的过程中只发生了化学变化
C. 从海水中可以得到NaCl,电解熔融NaCl可制备Cl2
D. 利用潮夕发电是将化学能转化为电解
15. 用CO还原M g Fe2O3,生成气体经冷却后通入过量石灰乳中,石灰乳增生P g,剩余固体N g. 已知氧的相对原子质量为16,设碳的相对原子质量为X,则X等于( )
A. 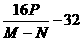 B.
B.
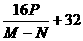 C.
C.
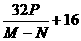 D.
D.

14. 化学在生产和日常生活中有着重要的应用。下列说法不正确的是( )
A. 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B. 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
C. MgO的熔点很高,可用于制作耐高温材料
D. 电解MgCl2饱和溶液,可制得金属镁
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com