
题目列表(包括答案和解析)
8.L、M、R、P、Q分别代表五种不同化合价的氮元素的物质,A、B代表两种含不同化合价的氯元素的物质(每种物质中,氮和氯元素的化合价只有1种),又知物质M中的氮元素的化合价比物质Q中氮元素的化合价低。在一定条件下,它们会发生如下的转化:
①P+A→Q+B ②L+O2→M+H2O
③L+M→R+H2O ④B+H2O→A+O2
(1)若五种含氮元素的物质中,有一种是硝酸,则硝酸是________,理由是________。
(2)反应②必须在催化剂(Pt、Fe2O3)等作用下,加热到一定温度时才能发生,此反应在化工生产中有重要用途。据此推断在同温、同压下,若物质R的密度比CO2的密度小,则R的化学式为________。
(3)某学生写出下面三个含氮物质的相互转化的关系式:
(a)M+P→N2O3+H2O (b)N2O4+H2O→P+Q (c)M+L→Q+H2O
其中一定不能实现的是________,理由是________________。
答案:(1)P;P在5种含N的物质中化合价最高 (2)N2 (3)(c);化合价L<M<Q
7.将某血液2.OmL用蒸馏水稀释后,往其中加入足量的(NH4)2C2O4(草酸铵)晶体,反应生成沉淀CaC2O4 。将沉淀用稀H2SO4处理得H2C2O4后,再用KMnO4溶液滴定(氧化产物为CO2,还原产物为Mn2+),结果用去了1.0×10-4mol/L的KMnO4溶液20.0mL,由此可知100mL该血液中的含钙量为( )。
A.5.0mg B.6.0mg C.10.0mg D.20.0mg
答案:C
6.(NH4)2PtCl6晶体受热完全分解,放出N2和HCl(气),同时还生成金属铂和NH4Cl,在此分解产物中,氧化产物与还原产物的物质的量之比是( )。
A.1:2 B.1:3 C.2:3 D.3:2
答案:C
5.向含有0.078mol的FeCl2溶液中通入0.009molCl2,再加入含0.02molX2O 的酸性溶液,使溶液中的Fe2+恰好全部氧化为Fe3+,并使X2O
的酸性溶液,使溶液中的Fe2+恰好全部氧化为Fe3+,并使X2O 还原为Xn+,则n值为( )。
还原为Xn+,则n值为( )。
A.2 B.3 C.4 D.5
答案:B
4.有关3BrF3 +5H2 O=HBrO3 +Br2 +9HF+ O2↑反应的叙述中,正确的是( )。
A.还原剂和氧化剂的物质的量之比为5:3 B.HBrO3和HF是还原产物
C.生成1molO2 ,转移6mol电子 D.BrF3既是氧化剂,又是还原剂
答案:D
3.用下列方法制取O2:①KClO3(MnO2)受热分解;②Na2O2加水;③H2O2中加MnO2;④KMnO4受热分解,若制得相同质量的O2,反应中上述各种物质(依编号顺序)的电子转移数目之比是( )。
A.3:2:2:4 B.1:1:1:1 C.2:1:1:2 D.1:2:1:2
答案:C
2.往浅绿色的Fe(NO3)2溶液中,逐滴加入稀HCl时,溶液的颜色变化应该是( )。
A.颜色变浅 B.逐渐加深 C.没有改变 D.变棕黄色
答案:D
1.铜和浓硝酸反应,若有0.1mol的电子发生转移,则被还原的硝酸是( )。
A.12.6g B.6.3g C.126g D.63g
答案:B
9.配平下列氧化还原反应方程式:
(1)( )Na2S2O3+( )HCl→( )NaCl+( )S+( )H2O+( )SO2↑
(2)( )Cr3++( )H2O2( )OH→( )CrO +( )H2O
+( )H2O
(3)( )Zn+( )H++( )NO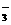 →(
)Zn2++(
)NH
→(
)Zn2++(
)NH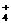 +( )H2O
+( )H2O
(4)( )HClO3+( )P+( )H2O→( )HCl+( )H3PO4
(5)( )P4+( )HNO3+( )H2O→( )H3PO4+( )NO↑
(6)( )Crl3+( )Cl2+( )KOH→( )K2CrO4+( )KIO4+( )KCl+( )H2O
答案:(1)1.2-2.1.1.1 (2)2.3.10-2.8 (3)4,10.1-4.1.3 (4)5.6.9-5.6
(5)3.20.8-12.20 (6)2.27.64-2.6.54.32
综合练习
8.已知反应S2O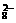 +2e-=2SO
+2e-=2SO ,Mn2++4H2O→MnO
,Mn2++4H2O→MnO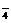 +8H++5e‑,则氧化ImolMn2+需S2O
+8H++5e‑,则氧化ImolMn2+需S2O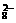 的物质的量为____________。Mn2+与S2O
的物质的量为____________。Mn2+与S2O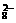 在水溶液中发生氧化还原反应的化学方程式为______________________________________________________。
在水溶液中发生氧化还原反应的化学方程式为______________________________________________________。
答案:2.5mol;2Mn2++5S2O82-+8H2O=10SO42-+2MnO4-+16H+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com