
题目列表(包括答案和解析)
4.某可逆反应A(气)+B(气)⇌C(气)。在两个完全相同的密闭容器中分别加入A、B各1mol,第一个容器温度为400℃,达到平衡时压强为原来的75%,第二个容器温度为600℃,达到平衡时A的体积百分含量为25%,通过计算推断该反应的正反应是吸热反应还是放热反应?
答案:经计算400℃时A的转化率为50%,600℃时A的转化率为67%。 该反应为吸热反应。
该反应为吸热反应。
3.把氮气和氢气按1:1(物质的量之比)混合后取四等份,同时充入A、B、C、D四个装有催化剂的真空密闭容器中,在保持相同温度的条件下,四个容器中的合成氨反应相继达到化学平衡状态,分析下表中数据并回答问题(用A、B、C、D)填空:
|
容器代号 |
A |
B |
C |
D |
|
平衡时混合物的平均相对分子质量 |
|
16 |
|
17 |
|
平衡时N2的转化率 |
|
|
20% |
|
|
平衡时H2的转化率 |
30% |
|
|
|
(1)都达平衡时,容器中NH3的百分数____________________最大。
(2)达到平衡时所需时间最长的是__________容器。
(3)四个容器的容积由小到大的排列次序是__________。
答案:(1)C (2)B (3)CDAB
2.在一定温度下,把2体积N2和6体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通(如图2-6),容器中发生以下反应:
N2+3H2⇌2NH3(正反应为放热反应)
若反应达到平衡后,测得混合气体为7体积、据此回答以下问题:
(1)保持上述反应温度不变,设d、6、c分别代表起始加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体中各物质的百分含量仍与上述平衡时完全相同,那么:
①若a=1,c=2。则b=__________。在此情况下,反应起始时将向__________方向进行(填“正”或“逆”)。
②若需规定起始时,反应向逆方向进行,则c的范围是__________。
答案:①3;逆反应 ②1<c≤4
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取措施是____________________。其原因是______________________________。
答案:降温;上述平衡向气体体积缩小的方向移动,即此反应向放热反应方向移动
1.将NO2,充入易传热材料制成的容器A、B中(如图2-5)进行2NO2⇌N2O4(正反应为放热反应)反应。始终保持温度与外界相等。A的容积固定不变,B的上盖可随容器内气体的压强变化而上、下移动,以保持内外压强相等。在同温同压条件下,将等量NO2充入始态体积相同的A、B中,反应同时开始。问:
(1)反应开始时.两容器中生成N2O4的速率υA__________υB(填“>”、“=”或“<”)原因是______________________________。
(2)两容器都达到平衡时,A、B中NO2的转化率aA__________aB(填“>”、“=”或“<”)原因是______________________________。
答案:(1)=;两容器的起始浓度相同
(2)<;相当于A达到平衡后,加压,平衡向正反应方向移动
13. 一密封体系中发生下列反应:N2+3H2⇌2H3(正反应为吸热反应)图2-4是某一时间段中反应速率与反应进程的曲线关系图:
一密封体系中发生下列反应:N2+3H2⇌2H3(正反应为吸热反应)图2-4是某一时间段中反应速率与反应进程的曲线关系图:
(1)处于平衡状态的时间段是____________________。
答案:t0-t1;t2-t4;t5-t6
(2)tl、t3、t4“时刻体系中发生了变化的条件分别是________________________________________。
答案:升高温度、加催化剂
(3)下列各时间段内,氨的百分含量最高的是__________。
 A.t0-t1 B.t2-t3
A.t0-t1 B.t2-t3
C.t3-t4 D.t5-t6
答案:A
拓展练习
2.25mol;≥0
(3)3x;≥0
12.某温度下,向某密闭容器中加入1molN2和3mo1H2,使之反应合成NH3,平衡后,测得NH3的体积分数为m。若温度不变,只改变起始加入量,使之反应重新达到平衡后,NH3的体积分数仍为m。若N2、H2、NH3的加入量用工x、y、z表示,应满足:
(1)温度、体积恒定时,若x=0,y=0,则z:___________________。
温度、压强恒定时,若x=0,y=0,则z:__________。
(2)温度、体积恒定时,若工x=0.75mol,则v:__________,z:__________;
温度、压强恒定时,若x=0.75mol,则y:__________,z:____________________。
(3)温度、压强恒定时,x、y、z应满足的关系是____________________。
答案:(1)2mol;>0
(2)2.25mol;0.5mol
11.反应nA(g)+mB(g)⇌pC(g)达到平衡后,当升高温度时,B的转化率变大,当减压后混合体系中C的百分含量减少(其他条件不变),试推测逆反应是____________反应,m+n___________________p(填“<”、“>”或“=”),当改变下列条件(其他条件不变)填入相应项目的变化情况。
答案:放热;>
(1)减压后,A的百分含量________________;
(2)加入B,A的转化率______________________;
(3)升温后,[D]/[C]将变__________________;
(4)降温时,混合气体的平均相对分子质量__________;
(5)使用催化剂,气体混合物的总物质的量__________。
答案:(1)增加 (2)增加 (3)减小 (4)减小 (5)不变
10.在容积相同且固定不变的四个密闭容器中,进行同样的可逆反应:2A(气)+B(气)⇌3C(气)+2D(气),起始时四个容器所盛A、B的量分别为
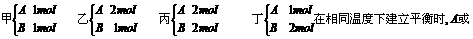 B的转化率大小关系中正确的是( )。
B的转化率大小关系中正确的是( )。
A.A的转化率:乙<丙<甲<丁 B.A的转化率:甲<乙<丙<丁
C. A的转化率:甲<乙二丙<丁 D.B的转化率:甲>丙>乙>丁
答案:A
9.图2-3表示外界条件(温度、压强)的变化对下列反应的影响L(固)+G(气)⇌2K(气)(正反应为吸热反应),在图中,y轴是指( )。
 A.平衡混合气中K的百分含量
A.平衡混合气中K的百分含量
B.平衡混合气中G的百分含量
C.G的转化率
D.L的转化率
答案:B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com