
题目列表(包括答案和解析)
1.下面列举了一些化合物的组成或性质,以此能够说明该化合物肯定属于有机物的是( )。
A.仅由碳、氢两种元素组成 B.仅由碳、氢、氧三种元素组成
C.在氧气中能燃烧,且只生成二氧化碳 D.熔点低且不溶于水
答案:A
2.化学实验员给某学生提供下列药品和必要的实验仪器,要求学生设计实验证明乙酸是弱酸,药品是冰醋酸、蒸馏水和pH试纸。此同学思考后认为:
(1)设计的理论依据是___________________________。
(2)实验简要步骤是___________________________。
(3)需记录的现象和数据是___________________________。
(4)推断与分析,由于__________________说明__________________,所以乙酸是弱酸。
答案:(1)弱电解质稀释10a 倍,pH改变小于a
(2)将一定浓度的乙酸稀释到一定量(如100倍体积)后,测量稀释前后的pH
(3)稀释的倍数、稀释前后溶液的pH
(4)溶液稀释100倍体积后,溶液pH值的改变小于2;稀释过程中乙酸的电离度增大
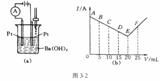
1.有一实验如图3-2(a)所示:
将30mL0.1mol/L的Ba(OH)2溶液置于烧杯中,然后边搅拌边慢慢加入0.1mol/L某第3周期元素形成的某酸溶液共25mL,加入酸的体积V和电流强度I的I-V图如图3-2(b)所示。
根据上述情况填写下列空白:
(1)此酸的化学式为__________________。
(2)处于C点时,溶液中导电的阳离子主要是___________________________。
(3)处于F点时,溶液中导电的阴离子主要是___________________________。
(4)烧杯中刚加入酸时,观察到的现象是___________________________。
(5)图b中,从A→E电流强度I变小的主要原因是__________________。
答案:(1)H3PO4 (2)Ba2+ (3)H2PO (4)有白色沉淀生成 (5)生成难溶的Ba3(PO4)2和难电离的水,使溶液中离子浓度降低
12.图3-1的图象是在一定温度下,向不同电解质溶液中加入新物质时溶液的导电性能发生变化,其电流强度(I)随新物质加入量(m)的变化曲线,以下四个导电性实验,其中与A图变化趋势一致的是_________,与B图变化趋势一致的是_________,与C图变化趋势一致的是__________________。

(1)Ba(OH)2 溶液中滴人H2SO4溶液至过量
(2)醋酸溶液中滴入NH3·H2O至过量
(3)澄清石灰水中通入CO2至过量
(4)NH4Cl口溶液中逐渐加入适量NaOH固体
 答案:(2); (1)(3); (4)
答案:(2); (1)(3); (4)
拓展练习
11.在下列三种溶液中①5mL 0.2mol/LCH3COOH ②5mL 0.1mol/LH2SO4 ③10mL 0.1mol/LHCI
(1)[H+]最大的是__________________。
(2)[H+]最小的是__________________。
(3)若用0.1mol/LNaOH溶液中和上述三种酸,所需NaOH溶液的体积分别是
①__________________、②__________________、③__________________。
答案:(1)② (2)① (3)①10mL②10mL③10mL
10.用足量的锌粉与稀H2SO4反应制H2时,由于反应速率太快难以控制,为了减慢反应速率,但不影响生成H2的总量,可向其中加入( )。
A.NaOH(固) B.Na2CO3(固) C.CH3COONa(固) D.K2SO4溶液
答案:CD
9.20℃时,H2S的饱和溶液1L,浓度约为1.0mol/L,其电离方程式为:
第一步:H2S⇌H++HS-
第二步:HS-⇌H++S2-
若使该溶液中[H+]减小的同时[S2-]也减小,可采用的措施是( )。
A.加入适量的NaOH B.加入适量的水
C.通人适量的SO2 D.加入适量CuSO4固体
答案:BC
8.有两种一元弱酸的钠盐溶液,其物质的量浓度相等。现向这两种盐的溶液中分别通入适量的CO2,发生如下反应:
NaR+CO2+H2O=HR+NaHCOO3
2NaR'+CO2+H2O=2HR'+Na2CO3
比较HR和HR',酸性的强弱,正确的是( )。
A.HR较弱 B.HR'较弱 C.两者相差不大 D.无法比较
答案:B
7.将0.1mol下列物质置于1L水中,充分搅拌后,溶液中阴离子数最多的是( )。
A.MgSO4 B.Mg(OH)2 C.BaO D.SO3
答案:C
6.某一元强酸X的溶液和某一元弱酸Y的溶液,它们的[H+]相等。将两种酸溶液各取50mL分别与足量镁屑反应。现有如下叙述:①X溶液与Y溶液的物质的量浓度相等 ②开始反应时两种溶液的反应速率相等 ③反应开始后X的反应速率下降较快 ④反应开始后Y的反应速率下降较快 ⑤完全反应后X产生的氢气较多 ⑥完全反应后Y产生的氢气较多。以上叙述中正确的是( )。
A.①②③⑤ B.①②④⑥ C.②④⑤ D.②③⑥
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com