
题目列表(包括答案和解析)
7.在一个容积为2L的密闭容器中,发生如下反应:3A+B⇌2C(A、B、C均为气体),若最初加入的A、B都是4mol,A的平均反应速率为0.12mol/(L·s),则10s后容器中的B是( )。
A.2.8mol B.1.6mol C.3.2mol D.3.6mol
答案:C
6.把选项中的四种x溶液,分别加进四个盛有10mL 2mol/L盐酸的烧杯中,并且均加水稀释至50mL,此时x和盐酸缓缓地进行反应,其中反应速率最快的是( )。
A.10mL 2mol/L B.20mL2mol/L C.10mL4mol/L D.20ml 3mol/L
答案:D
5.反应4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)在10L的密闭容器中进行,30s后水蒸气的物质的量增加了0.45mol,则此反应的平均速率υ(X)可表示为( )。
A.υ(NH3)=0.010mol/(L·s) B.υ(O2)=0.0010mol/(L·s)
C.υ(NO)=0.001 0mol/(L·s) D.υ(H2O)=0.045mol/(L·s)
答案:C
4.下列说法中错误的是( )。
A.化学反应的过程包含旧键的分裂和新键的生成
B.反应物的性质和反应条件都会影响化学反应速率
C.能够发生碰撞的分子叫活化分子
D.能发生化学反应的碰撞叫有效碰撞
答案:C
3.在可逆反应中,混合物各成份的浓度比一定等于化学计量数之比的是( )。
A.起始浓度 D.转化浓度 C.平衡浓度 D.都不等于
答案:B
2.盐酸与Na2CO3反应时,能使反应的最初速率明显加快的是( )。
A.增加Na2CO3粉末的量 B.增加盐酸的量一倍
C.盐酸浓度加倍用景减半 D.温度升高40℃
答案:CD
1.化学反应速率是指( )。
A.反应物浓度的减少
B.生成物浓度的增加
C.单位时间内反应物浓度的减少或生成物浓度的增加
D.某一时刻生成物物质的量
答案:C
18.废金属应当回收利用。下面是利用废铜屑生成胆矾的流程:
废铜屑 铜屑
铜屑 氧化铜
氧化铜 溶液
溶液 胆矾(CuSO4·5H2O)
胆矾(CuSO4·5H2O)
现有含铜质量分数为98%的废铜屑100kg,若在整个制备过程中铜的损耗为1%,计算可制得胆矾的质量。
答案:379.0kg
17.制取氨气并完成喷泉实验。
(1)写出实验室制取氨气的化学方程式________________________。
(2)用图工装置进行喷泉实验时,上部烧瓶已装满了氨气,引发水上喷的操作是________________________________,该实验的原理是________________________。
(3)如果只提供图Ⅱ的装置,请说明引发喷泉的方法________________________________。
答案:(1)2NH4CI+Ca(OH)2 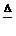 2NH3↑+2H2O+CaCl2;
2NH3↑+2H2O+CaCl2;
(2)打开止水夹,挤出胶头滴管中的水;氨气极易溶于水,致使烧瓶内气体压强迅速减小;
(3)打开夹子,用手(或热毛巾)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管中的空气,氨气与水接触,即发生喷泉
16.拟用下图1-13装置制取表中的三种干燥纯净的气体(图中的铁架台、铁夹、加热及气体收集装置均已略去,必要时可加热;a、b、c、d表示相应仪器中加入的试剂)。
|
气休 |
a |
b |
c |
d |
|
Cl2 |
浓盐酸 |
MnO2 |
NaOH溶液 |
浓H2SO4 |
|
NH3 |
饱合NH4Cl溶液 |
消石灰 |
H2O |
固体NaOH |
|
NO |
稀HNO3 |
Cu屑 |
H2O |
P2O5 |
(1)上述方法可得干燥纯净的气体是________。
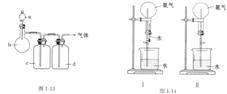 (2)指出不能用上述方法制取的气体,并说明理由(可以不填满)。
(2)指出不能用上述方法制取的气体,并说明理由(可以不填满)。
①气体________,理由是________________________________。
②气体________,理由是________________________________。
③气体________,理由是________________________________。
答案:(1)NO
(2)①Cl2;反应生成的 被C中的NaOH溶液吸收
被C中的NaOH溶液吸收
②NH3;反应生成的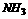 被C中的H2O吸收
被C中的H2O吸收
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com