
题目列表(包括答案和解析)
28. 已知某有机物的结构简式为:
已知某有机物的结构简式为:
(1)该有机物中的含氧官能团的名称为 。
(2)该有机物发生加成聚合反应后,所得产物的结构简式为 。
(3)写出该有机物发生消去反应的化学方程式:
。
27.根据下列4组物质的结构简式回答:
① CH4和CH3CH3 ② CH2=CHCH3 和CH3CH=CH2
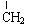 ③ CH3CH2CH2CH3和CH3CHCH3 ④ C2H5OH和CH3OCH3
③ CH3CH2CH2CH3和CH3CHCH3 ④ C2H5OH和CH3OCH3
(1)属于同系物的是 (填序号,下同)。
(2)属于同一物质的是 。
(3)具有不同官能团的同分异构体是 。
(4)由于碳链骨架不同而产生的同分异构体是 。
26.有机化学中的反应类型较多,将下列反应归类(填序号)。
①由乙炔制氯乙烯 ②乙烷在空气中燃烧③乙烯使溴的四氯化碳溶液褪色
④乙烯使酸性高锰酸钾溶液褪色 ⑤由乙烯制聚乙烯
⑥甲烷与氯气在光照的条件下反应 ⑦溴乙烷和氢氧化钠乙醇溶液共热
⑧溴乙烷和氢氧化钠溶液共热
其中属于取代反应的是________;属于氧化反应的是.________;属于加成反应的是.________;属消去反应的是________;属于聚合反应的是__________ 。
请写出⑤⑥⑦⑧的化学反应方程式。
⑤_________________________________________________
⑥_________________________________________________
⑦_________________________________________________
⑧_________________________________________________
23、已知某金属晶体是面心立方堆积,金属原子的半径为a pm,摩尔质量为Mg/mol,阿伏加德罗常数为NA
求(1)该晶胞中含有原子的个数?
(2)该金属的密度(用a、M、NA来表示)
(3)空间利用率为多少?

22、(9分)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
|
元 素 |
Mn |
Fe |
|
|
电离能 /kJ·mol-1 |
I1 |
717 |
759 |
|
I2 |
1509 |
1561 |
|
|
I3 |
3248 |
2957 |
回答下列问题:
⑴ Mn元素价电子层的电子排布式为 ,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。对此,你的解释是
;
⑵ Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物。
① 与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 ;
② 六氰合亚铁离子(Fe(CN)64-)中的配体CN-中C原子的杂化轨道类型是 ,写出一种与CN-互为等电子体的单质分子的结构式 ;
⑶ 三氯化铁常温下为固体,熔点282℃,沸点315℃,
在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮
等有机溶剂。据此判断三氯化铁晶体为 ;
⑷ 金属铁的晶体在不同温度下有两种堆积方式,晶胞
分别如右图所示。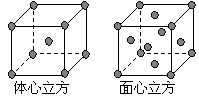 面心立方晶胞和体心立方晶胞中实际
面心立方晶胞和体心立方晶胞中实际
含有的Fe原子个数之比为
。
21、(15分)五种短周期元素A、B、C、D、E,原子序数依次增大,其中A、B同周期,且A、B原子核外均有两个未成对电子;A、D同主族,B、E同主族,且C的最外层电子比E的最外层电子少5个。根据以上信息,完成下列各题。
(1)写出下列化学用语:A: B: C: D: E:
(2)A的最高价氧化物的熔点 D的最高价氧化物的熔点(填“>”或“<”),原因是 ;B氢化物的沸点 E氢化物的沸点(填“>”或“<”),原因是 。
(3)选取上述五种元素,完成下列问题
①构成的原子晶体有 ;(写化学式)
②含有极性键的非极性分子 (用电子式表示)
20、(6分)下表是元素周期表的一部分。
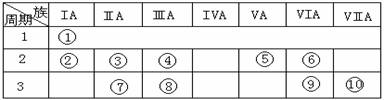
(1)表中元素⑩的氢化物的化学式为 ,此氢化物的还原性比元素⑨的氢化物的还原性 (填强或弱)
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是 ,其氢化物的电子式为 。
(3)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式
19、(10分)为了比较温室效应气体对目前全球增温现象的影响, 科学家通常引用“温室效应指数”,以二氧化碳为相对标准。表1有(A)至(I)共九种气体在大气中的体积百分比及其温室效应指数。
结合表中列出的九种气体,试参与回答下列各题:
|
选项 |
物质 |
大气中的含量(体积百分比) |
温室效应指数 |
|
A |
N2 |
78 |
0 |
|
B |
O2 |
21 |
0 |
|
C |
H2O |
1 |
0.1 |
|
D |
CO2 |
0.03 |
1 |
|
E |
CH4 |
2×10-4 |
30 |
|
F |
N2O |
3×10-5 |
160 |
|
G |
O3 |
4×10-6 |
2000 |
|
H |
CCl3F |
2.8×10-8 |
21000 |
|
I |
CCl2F2 |
4.8×10-8 |
25000 |
(1)下列由极性键形成的极性分子是 。
A.N2 B.O2 C.H2O D.CO2 E.CH4
(2)下列说法不正确的是 。
A.N2O与CO2, CCl3F与CCl2F2互为等电子体
B.CCl2F2无同分异构体,说明其中碳原子采用sp3方式杂化
C.CH4是目前引起温室效应的主要原因
D.H2O沸点是九种物质中最高的,是因为水分子间能形成氢键
(3)在半导体生产或灭火剂的使用中,会向空气逸散气体如:NF3、CHClFCF3、C3F8,它们虽是微量的,有些确是强温室气体,下列推测不正确的是 。
A.由价层电子对互斥理论可确定NF3分子呈三角锥形
B. C3F8在CCl4中的溶解度比水中大
 C.CHClFCF3存在手性异构
C.CHClFCF3存在手性异构
D.第一电离能:N<O<F
(4)甲烷晶体的晶胞结构如右图,下列有关说法正确的是 。
A.甲烷在常温下呈气态,说明甲烷晶体属于分子晶体
B.晶体中1个CH4分子有12个紧邻的甲烷分子
C. CH4晶体熔化时需克服共价键
D.可燃冰(8CH4·46H2O)是在低温高压下形成的晶体
(5)水能与多种过渡金属离子形成络合物,已知某红紫色络合物的组成为CoCl3·5NH3·H2O。其水溶液显弱酸性,加入强碱并加热至沸腾有氨放出,同时产生Co2O3沉淀;加AgNO3于该化合物溶液中,有AgCl沉淀生成,过滤后再加AgNO3溶液于滤液中无变化,但加热至沸腾有AgCl沉淀生成, 且其质量为第一次沉淀量的二分之一。则该配合物的化学式最可能为 。
A. [ CoCl2(NH3)4 ]Cl·NH3·H2O; B. [ Co(NH3)5(H2O)]Cl3 ;
C. [ CoCl2(NH3)3(H2O)]Cl·2NH3 ; D. [ CoCl(NH3)5]Cl2·H2O。
(6)题(5)中钴离子在基态时核外电子排布式为: 。
18、2001年报道硼和镁形成的化合物刷新了金属化合物超导温度的最高记录。如右下图是该化合物
的晶体结构单元:镁原子间形成正六棱柱,且棱柱的上下面还各有一个镁原子;6个硼原子位于棱
的侧棱上,则该化合物的化学式可表示为
A.MgB B.Mg3B2 C.MgB2 D.Mg2B3
第Ⅱ卷(非选择题)
17.据下列给出几种物质的熔点和沸点判断下列有关说法中错误的是
|
|
NaCl |
MgCl2 |
AlCl3 |
SiCi4 |
 单质B 单质B |
|
熔点 |
810℃ |
710℃ |
190℃ |
-68℃ |
2300℃ |
|
沸点 |
1465℃ |
1418℃ |
182.7℃ |
57℃ |
2500℃ |
A.SiCl4是分子晶体 B.单质B是原子晶体
C.AlCl3加热能升华 D.MgCl2所含离子键的强度比NaCl大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com