
题目列表(包括答案和解析)
3.下列离子中,氧化能力最强的是( )。
A.Fe3+ B.Cu2+ C.H+ D.Fe2+
答案:A
2.下列物质中,能溶于稀H2SO4,且放出气体的是( )。
A.AgCI B.FeS C.CaCO3 D.BaSO4
答案:B
1.下列各物质中,在一定条件下,不能由两种单质直接化合制得的是( )。
A.FeS B.Fe3O4 C.CuS D.FeCl2
答案:CD
5.实验室用空气和图4-4所示药品、仪器装置制取少量氮化镁。
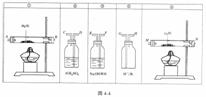
(1)如果所制气体从左向右流向时,上述仪器装置正确连接顺序是___________(填装置序号)。
(2)各个装置中导管连接的顺序正确的是H→___________,E→___________,C→___________,N→___________。
(3)实验开始时,应先在___________处接通自来水管,然后依次点燃装有___________粉装置的酒精灯和装有___________粉装置的酒精灯。
(4)装置②中浓H2SO4的作用是___________;装置③中饱和NaOH溶液的作用是___________,装置⑤的作用是___________。
(5)实验装置N处的气体是___________,装置①中发生反应的化学方程式是___________。
答案:(1)④③②⑤① (2)F; D;M;A
(3)G;Cu;Mg (4)除去空气中的水蒸气;除去空气中的CO2;除去空气中的O2 (5)N2;3Mg+N2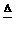 N2
N2
4.在化工生产中,要用一种无色可溶于水的晶体--铝铵矾。该晶体是一种复盐,其主要成份为十二水合硫酸铝铵。向该复盐的溶液中逐滴加入浓NaOH溶液,将发生一系列的变化,已知NH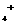 和A1O2-在水溶液中不能大量共存,会发生下列反应:
和A1O2-在水溶液中不能大量共存,会发生下列反应:
NH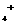 +A1O
+A1O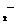 +H2O=Al(OH)3+NH3↑
+H2O=Al(OH)3+NH3↑
试回答:
(1)硫酸铝铵在水溶液中的电离方程式为___________。
(2)在逐滴加入浓NaOH溶液的过程中,产生的现象有:①溶液中出现白色沉淀 ②有刺激性气味的气体逸出 ③白色沉淀量逐渐增多 ④白色沉淀完全消失 ⑤白色沉淀量逐渐减少。
请回答各种现象由先到后出现的顺序(用序号回答)______________________。
(3)写出滴人NaOH溶液的过程中,有关反应的离子方程式。
①______________________; ②______________________; ③______________________。
答案:(1)NH4(SO4)2=NH4+ +Al3++2SO42-
(2)①→③→②→⑤→④
(3)化学方程式略
3. 氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
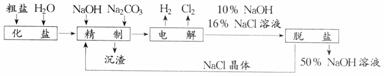
(1)工业食盐中含有Ca2+、Ng2+和SO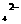 ,为了有效地除去它们,加入试剂的合理顺序是( )。
,为了有效地除去它们,加入试剂的合理顺序是( )。
a.先加NaOH,后加Na2CO3,再加钡试剂。
b.先加NaOH,后加钡试剂,再加Na2CO3。
c.先加钡试剂,后加NaOH,再加Na2CO3。
(2)脱盐工序中利用NaOH和NaCI在溶解度上的差异,通过___________、冷却、___________(填写操作名称)除去NaCl。
(3)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH溶液反应;采用无隔膜电解冷的食盐水时,C12和NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为______________________。
答案:(1)b、c (2)蒸发;过滤
(3)NaCl+H2O NaClO+H2↑
NaClO+H2↑
2.如图4-3所示,在含有1molMg2+和1molAl3的混合溶液中,现按横坐标依次加入NaOH溶液、盐酸,通入CO2气体,纵坐标为混合沉淀物的物质的量,请画出沉淀的物质的量随反应变化的曲线,并写出各步反应的离子方程式。
答案:略
1.已知向含有Zn2+的溶液中滴加氨水,有白色沉淀生成,继续滴加氨水使其过量,则沉淀又溶解,生成[Zn(NH3)4]2+。此外Zn(OH)2既可溶于盐酸,又可溶于NaOH溶液,生成ZnO22-,所以Zn(OH)2是一种两性氢氧化物。
现有四组离子,每组有两种金属离子。请各选出一种试剂,将它们两者分开。可选择的试剂有:
A.H2SO4 B.HCl C. HNO3 D.NaOH E.氨水
根据上述内容填写下表:
|
离子组 |
选用试剂 |
沉淀物化学式 |
保留溶液中离子 |
|
(1)Zn2+和Al3+ |
|
|
|
|
(2)Zn2+和Mg2+ |
|
|
|
|
(3)Zn2+和Ba2+ |
|
|
|
|
(4)Mg2+和Al3+ |
|
|
|
答案:(1)E;Al(OH)3;[Zn(NH3)4]2+ (2)D;Mg(OH)2;ZnO22-或E;Mg(OH)2;[Zn(NH3)4]2+ (3)A;BaSO4;Zn2+ (4)D;Mg(OH)2;A1O2-
16.把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量的水中有0.58g白色沉淀。在所得溶液中逐滴加入0.5mol/L的盐酸,加入盐酸的体积与生成沉淀的质量如图4-2所示:
(1)混合物中MgCl2的质量为___________;
 (2)混合物中AlCl3的质量为___________;
(2)混合物中AlCl3的质量为___________;
(3)混合物中的NaOH的质量为___________;
(4)P点表示的盐酸体积为___________。
(沉淀开始增加时盐酸加入量为 10mL,沉淀量最大时,加入盐酸的体积为30mL)
答案:(1)0.95g (2)1.335g (3)2.6g (4)130mL
拓展练习
15.当mmLbmol/L的A1Cl3溶液中加入等体积的amol/LNaOH溶液。
(1)当d≤3b时,生成Al(OH)3沉淀的物质的量为___________mol;
(2)当d、b满足___________条件时,无沉淀生成;
(3)当a、b分别满足___________、___________条件时,有沉淀生成,生成Al(OH)3沉淀的物质的量分别是; ___________和___________。
答案:(1)≤ (2)d≥4b (3)a≤3b;3b<a<4b;26a×l0-3 ;78(46m-am)×10-3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com