
题目列表(包括答案和解析)
3.下列叙述正确的是( )
A.常见金属铁和铝在工业上是由热还原法制得的
B.二氧化硅晶体被广泛用于制作太阳能电池和光导纤维
C.玛瑙和餐桌上的瓷盘都是硅酸盐制品
D.钢材和硬币都是合金,若改变这些合金的原料配比会改变这些合金的性能
2. 下列各组干燥气体和溶液,其中可以进行喷泉实验,且液体几乎充满烧瓶的是( )
下列各组干燥气体和溶液,其中可以进行喷泉实验,且液体几乎充满烧瓶的是( )
A.Cl2,饱和食盐水 B.CO2,碳酸氢钠溶液
C.SO2,稀氨水 D.NO2,水
1.随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品氧化变质,在包装袋中可以放入的化学物质是( )
 A.无水硫酸铜 B.硫酸亚铁 C. 食盐 D. 生石灰
A.无水硫酸铜 B.硫酸亚铁 C. 食盐 D. 生石灰
33. 甲醇是一种可再生能源,具有广泛的开发和应用前景。在容积为2L的密闭容器中充入
lmol
CO与2molH2在催化剂作用下反应生成甲醇: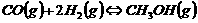 , CO
, CO
平衡转化率与温度、压强的关系如意图所示;
(1) Pl____P2(填大于、小于或等于)
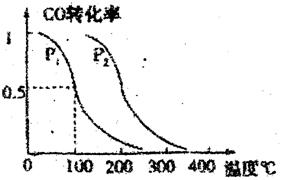 (2) 若Pl为1标准大气压,反应温度为100℃,此
(2) 若Pl为1标准大气压,反应温度为100℃,此
条件下反应达到平衡:
①达到平衡所需的时间为5min,用H2表示的平
均反应速率为________。
②反应的平衡常数K= 。
③平衡时,测得其能量的变化量为akJ。则该
反应的热化学方程式是:
。
(3) 恒容恒温情况下,再增加lmol CO与2molH2,达到新平衡时.CO的转化率 .
(填“增大”、“减小”或“不变”),平衡常数____。(填“增大”、“减小”或“不变”)
(4) 为了寻找一定催化剂下合成甲醇的适宜温度条件,某同学设计了一组实验,该实验中
应控制的不变量是 。
32.(16分)
Ⅰ. 现有①0.2mol/L NaOH溶液和②0.2mol/L HX溶液,两溶液等体积混合后,测得溶液中
c(Na+)>c(X-):
(1) 混合液显 性(填“酸”、“碱”或“中”),其原因用离子方程式表示
。
(2) 上述混合液中:(填“>”、“=电”或“<”)
c(Hx) c(X-); c(OH-) c(HX)+c(H+)
Ⅱ.下图是一个用铂丝作电极,电解稀的MgS04溶液的装置,电解液中滴有酚酞试剂,回答
下列问题;
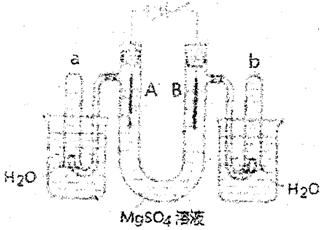
(1) 通电时,A管中的现象是 。
(2) ①通电时,A管中发生的反应方程式: 。
②通电时,B管中发生的反应方程式: 。
3. 溶液Z的pH影响聚铁中铁的质量分数,用PH试纸测定溶渡pH的操作方法为
。
21. (16分)聚合硫酸铁又称聚铁,化学式为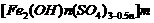 ,广泛用于污水处理。
,广泛用于污水处理。
某化学兴趣小组在实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、Si02等)
制备聚铁和绿矾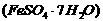 的过程如下:
的过程如下:
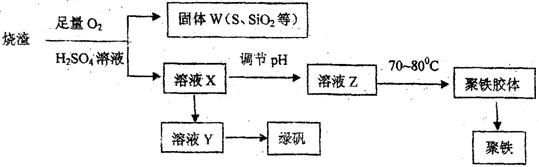
(1) 验证固体W焙烧后产生的气体含有SO2的方法是 。
(2) 实验室制各、收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各
仪器接口,顺序为a→ → → → →f,装置D的作用是
,装置E中NaOH溶液的作用是 。

(3) 制备绿矾时,内溶液X中加入过量 ,充分反应后,经
操作得到溶液Y,再经浓缩,结晶等步骤得到绿矾。
说明、方程式和重要演算步骤,只写出最后答案的不能得分。有数值计算的题,答案中
必须明确写出数值和单位。
30.(16分)有关元素X、Y、Z、W的信息如下:

请回答下列问题:
(1) 写出Y元素在元素周期表的位置 。
(2) W的单质与Y的最高价氧化物对应的水化物反应的离子方程式为 。
(3) 铜片、碳棒和ZX3溶液组成原电池,写出正极发生的电极反应方程式 。
(4) 向淀粉碘化钾溶液中滴加儿滴浓ZX3溶液,现象为 ,
写出反应的离子方程式 。
(5) 以WX3溶液为原料制取WX3·6H20溶液,主要的实验操作是 ,
以WX3·6H20晶体制取无水WX3,应在 条件下加热WX3·6H20晶体,
其原因是 (结合离子方程式简要说明)。
23. 下列方程式书写正确的是
A. KHC03的水解: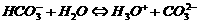
B. KHC03溶液与Al2(SO4)3溶液混合: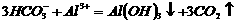
C.将过量铁粉加入到稀硝酸中;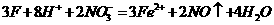
D.碳酸电离: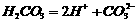
有两个选璜符合题目要求,全选对的得6分,只选1个且正确的得3分,有选错或不答
的得O分。
22. 下列溶液中有关物质的量浓度关系或计算正确的是
A. pH相等的NaOH、CH3COONa和NaHC03三种溶液,则有
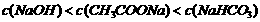
B.已知25℃时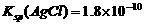 ,则在0.1mol·L-1AlCl3溶液中,Ag+的物质的
,则在0.1mol·L-1AlCl3溶液中,Ag+的物质的
量浓度最大可达到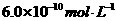
C.25℃时,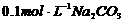 溶液中水电离出来的c(OH-)大于
溶液中水电离出来的c(OH-)大于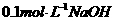
溶液中,水电离出来的c(OH-)
D. 室温下,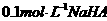 溶液的pH=4,则
溶液的pH=4,则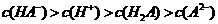
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com