
题目列表(包括答案和解析)
6.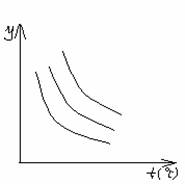 如图表示外界条件(温度、压强)的变化对反应影响, L(固)+G(气)
如图表示外界条件(温度、压强)的变化对反应影响, L(固)+G(气) 2R(气)– Q(Q>0),在图中,y轴指:
2R(气)– Q(Q>0),在图中,y轴指:
|
A.平衡混合气中R的百分含量 |
|
B.平衡混合气中G的百分含量 |
|
C.G的转化率 |
|
D.L的转化率 |
5.
在密闭容器中发生反应:aX(气)+bY(气) cZ(气)+dW(气)反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列叙述中不正确的是:
cZ(气)+dW(气)反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列叙述中不正确的是:
|
A.平衡向逆反应方向移动 |
B.a + b > c + d |
|
C.Z的体积分数增加 |
D.X的转化率下降 |
|
|
|
4.
在一定温度下的定容密闭容器中,当下列物理量不再变化时,表明反应
A(固)+2B(气) C(气)+D(气)已达平衡的是:
C(气)+D(气)已达平衡的是:
|
A.混合气体的压强 |
B.混合气体的密度 |
|
C.B的物质的量浓度 |
D.气体的总物质的量 |
3. 把下列A、B、C、D、四种不同体积和浓度的X溶液分别加入四个盛有10ml、2mol/l盐酸的烧杯中,并加水稀释至50ml,此时X和盐酸进行反应,其中反应速率最大的是:
|
A.10ml,4mol/l |
B.10ml,2mol/l |
C.20ml,3mol/l |
D.20ml,2mol/l |
2. 已知4NH3+5O2=4NO+6H2O,若反应速率分别用VNH3,VO2,VNO,VH2O [mol/(l·min)]表示,则正确的关系是:
|
A.4 VNH3=5 VO2 |
B.5 VO2=6 VH2O |
C.3VNH3=2 VH2O |
D.4 VO2=5 VNO |
1.
在N2+3H2  2NH3的反应中,经过一段时间后,NH3的浓度增加了0.6mol/l,在此段时间内用H2表示的平均反应速率为0.45mol/(l·s),则此段时间是:
2NH3的反应中,经过一段时间后,NH3的浓度增加了0.6mol/l,在此段时间内用H2表示的平均反应速率为0.45mol/(l·s),则此段时间是:
|
A.1s |
B.2s |
C.0.44s |
D.1.33s |
6. CH4在一定条件下经催化氧化可以生成C2EH2 和C2H4,现取一定量的CH4,经上述催化氧化后得到混和气体,它在标准状况下的密度为0.7698克/升。已知反应中CH4消耗了20%,计算混和气体中C2H2的体积百分含量(保留三位有效数字)。
5. 已知某混和气体的体积百分组成中有80.0%的CH4、15.0%C2H2、5.0%的C2H4,
请计算0.5摩尔该混和气体的质量和在标准状态下的密度(克/升)。
[解答]:
4. 取50.0毫升Na2CO3 和Na2S 的混和溶液,加入过量的AgNO3 溶液后,得到3.86克
沉淀;用过量的稀醋酸处理后,沉淀量减少到2.48克,并有气体放出。
请计算:
(1) 原混和溶液中Na2CO3 的摩尔浓度是( )摩/升.
Na2S 的摩尔浓度是( )摩/升。
[解答]:
(2) 产生的气体在标准状态下的体积。( )升。
[解答]:
3. 虽然有机化合物A、B的分子式不同,但它们所含元素只可能是碳、氢、氧中的两种或三种。如果将A、B以任何一种比例混合,只要其物质的量之和不变,完全燃烧时所消耗的氧气和生成的水的物质的量也不变,则A、B组成必须满足的条件_______________________。
[解答]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com