
题目列表(包括答案和解析)
11.等物质量的Na2CO3·mH2O和BaCl2·nH2O的混和物3.68克,加足量水搅拌,充分反应后可得到1.97克沉淀,则m和n的值分别为-----------------------(A)
A.1和2 B.1和3 C.7和3 D.10和2
[提示]:1.97克BaCO3其物质的量为0.01摩,所以Na2CO3·mH2O和BaCl2·nH2O也各为0.01摩,则有:0.01×(106+18m)+0.01×(208+18n) = 3.68,整理得:m+n=3
10.向含有a摩Ca(OH)2的澄清石灰水(未饱和)中通入b摩CO2,充分反应后,下列判断正确的是-----------------------------------------------------------------------(CD)
A.当a³b时,产生a摩沉淀 B.当a£b时,产生b摩沉淀
C.当a<b<2a时,产生2a-b摩沉淀 D.当2a<b时,溶液仍澄清
[提示]:aCa(OH)2+bCO2 = xCaCO3¯+yCa(HCO3)2
根据钙元素守恒,得:x+y=a, 根据碳元素守恒,得x+2y=b,解得x(CaCO3)为2a-b。
9.在化合物X2Y和YZ2中,Y的质量分数分别为40%和50%,则在化合物X2YZ3中Y的质量分数约为------------------------------------------------------------(B)
A.20% B.25% C.30% D.35%
[提示一]: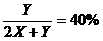
 解得X、Y后,再代入到
解得X、Y后,再代入到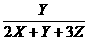 可得结果,但过程太繁
[提示二]:Y在X2Y中的原子量为40,则X的原子量为30;在YZ2中,Y的原子量若为40,则Z的原子量为20(因为Y占50%)。故化合物X2YZ3中:
Y% =
可得结果,但过程太繁
[提示二]:Y在X2Y中的原子量为40,则X的原子量为30;在YZ2中,Y的原子量若为40,则Z的原子量为20(因为Y占50%)。故化合物X2YZ3中:
Y% = 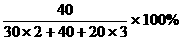 = 25%
[提示三]:由X2Y中Y占40%,即可令X=3,Y=4;又由YZ2中Y占50%,则有Y=2Z,即Z=2,于是
= 25%
[提示三]:由X2Y中Y占40%,即可令X=3,Y=4;又由YZ2中Y占50%,则有Y=2Z,即Z=2,于是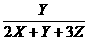 =
= 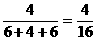 ,即B
[提示四]:由于题中给出X2Y中Y的质量分数为40%,设Y的相对原子量为a,可以解得X的相对原子量为0.75a,那么Z的相对原子质量为0.5a, 把这三个假设的原子质量代入X2YZ3中,易求出Y的质量分数为25%
,即B
[提示四]:由于题中给出X2Y中Y的质量分数为40%,设Y的相对原子量为a,可以解得X的相对原子量为0.75a,那么Z的相对原子质量为0.5a, 把这三个假设的原子质量代入X2YZ3中,易求出Y的质量分数为25%
8.已知一个SO2 的分子的质量为n千克,一个SO3
分子的质量为m千克,若以硫原子的质量的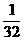 作为原子量的标准,则SO3的分子量( C )
作为原子量的标准,则SO3的分子量( C )
A.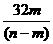 B.
B.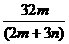 C.
C. D.
D.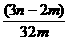
[提示]:硫原子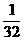 的标准与碳原子的
的标准与碳原子的 的标准完全一样.
的标准完全一样.
7.用H2还原CuOm克,先加热且待冷却后,称得剩余固体为n克,共用去H2W克,则参加反应的CuO的百分比为-----------------------------------------------------(D)
A.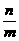 ×100% B.
×100% B. ×100% C.
×100% C.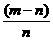 ×100% D.
×100% D. ×100%
×100%
[提示]:不少学生可能会把B也选进去,其实,用去“用去”与“参加反应”是不同的,“用去”的不一定是参加反应的,考虑到气体与固体反应时,气体总是不能完全参加反应这个事实,我们不应该把B作为答案。
6.已知阿佛加德罗常数、物质的摩尔质量及摩尔体积,下列物质量中尚不能全部计算出其近似值的是----------------------------------------------------------------(C)
A.固体物质分子的大小和质量 B.液态物质分子的大小和质量
C.气体物质分子的大小和质量 D.气体物质分子的质量
5.在等物质的量的短周期元素A和B中,分别加入足量的酸,在A中加入盐酸,B中加入稀硫酸,反应完全后,生成氢气的体积分别为VA和VB,且VA¹VB,若要确定反应生成物中A和B的化合价,至少还需知道和数据是--------------------(A)
A. VA:VB值 B. VA或VB的值
C.A或B的物质的量 D.盐酸和硫酸的摩尔浓度
[提示]:产生的氢气越多,化合价越高,金属与酸反应放出氢气,其化合价最高不会超过+3,故此不会出现+1:+2等价于+2:+4的情况
4.由甲烷、氨气、氢气组成有的混和气体的平均分子量为10,则混和气体中三者的体积比为---------------------------------------------------------------------------(D)
A.3:2:1 B.1:2:3 C.1:3:4 D.2:3:4
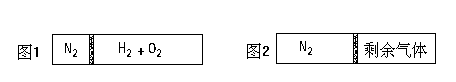
3.在20℃时,在一刚性容器内部有一个不漏气且可滑动的活塞将容器分隔成左右两室。左室充入氮气,右室充入氢气与氧气的混和气体,活塞恰好停留在离左端的 处(图1),然后引燃氢、氧混和气体,反应完毕后恢复至原来温度,活塞恰好停在中间(图2),如果忽略水蒸气体积,则反应前氢气与氧气的体积比可能是-(BD)
处(图1),然后引燃氢、氧混和气体,反应完毕后恢复至原来温度,活塞恰好停在中间(图2),如果忽略水蒸气体积,则反应前氢气与氧气的体积比可能是-(BD)
A.3:4 B.4:5 C.2:1 D.7:2
[提示]:设氮气的量为1体积,则氢、氧混和气体为3体积;从图示可以看出,反应后剩余的H2(或O2)也为1体积,如设参加反应的H2和O2分别为2x、x体积,有2x+x+1=3,解得x=
(1)如果H2有剩余,V(H2)=2x+1=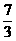 , V(O2)=x=
, V(O2)=x= , V(H2):V(O2)=7:2
, V(H2):V(O2)=7:2
(2)如果O2有剩余, V(H2)=2x=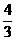 , V(O2)=x+1=
, V(O2)=x+1=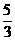 , V(H2):V(O2)=4:5
, V(H2):V(O2)=4:5
2.在化合物X2Y和YZ2中,Y的质量百分比分别为40%和50%,则在化合物X2YZ3中,Y的质量百分比为---------------------------------------------------(B)
A.20% B.25% C.30% D.70%
[解答]:在X2Y中,有 =40%----------①
=40%----------①
在YZ2中,有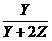 =50%------------②
=50%------------②
由①、②式可知2Z=Y。
在X2YZ3中,Y的质量百分比为Y%=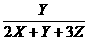 ,取其倒数为
,取其倒数为
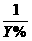 =
=
 =
=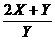 +
+ =
=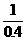 +
+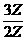 =4
=4
所 以 ,Y%= =25%
=25%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com