
题目列表(包括答案和解析)
10.把1克含脉石(SiO2)的黄铁矿样品在空气中灼烧,反应后得残渣0.78克,此黄铁矿的纯度是[答:66%]。 [提示]:2FeS2 - Fe2O3 DW
240 160 80 ?=0.66 0.22
9.将等物质的量的Cl2和SO2气体通入滴有石蕊试液的BaCl2溶液中,出现的现象是[答:产生白色沉淀,试液变成红色]。
8.在2FeS+6H2SO4(浓)  Fe2(SO4)3+3SO2↑+2S↓+6H2O反应中,[答:FeS]是还原剂,氧化产物和还原产物的质量比为[答:29:12]。
[提示]:Fe2(SO4)3也是氧化产物
Fe2(SO4)3+3SO2↑+2S↓+6H2O反应中,[答:FeS]是还原剂,氧化产物和还原产物的质量比为[答:29:12]。
[提示]:Fe2(SO4)3也是氧化产物
7.为降低硫的氧化物对空气的污染,可把氧化钙和含硫的煤混和后燃烧,这种方法叫做钙基固硫,试写出有关的化学方程式 [答:S+O2 == SO2 2CaO+2SO2+O2 == 2CaSO4]
6.工业上制取CuSO4不是直接用浓硫酸与铜反应,而是将铜丝浸入稀硫酸中并不断由容器的下部吹入细小的空气泡,试分析这种制备办法的优点。 [提示:这种办法的优点主要有两处:一是不产生污染空气的二氧化硫,二是提高了硫酸的利用率]
5.某热电厂地处多雨地带,使用的燃料煤中含有少量的硫,燃烧的气体未经处理即排放到空气中,又有部分发电用水未经冷却排入附近的河中,经观察其下游几十公里范围内的河水中鱼类几乎绝迹,试解释出现这种现象的原因。
[答:煤燃烧后,硫转化成二氧化硫气体,形成酸雨使何水酸度增大,排出的热水又使河水的温度升高,O2的溶解度降低,鱼类在这种环境中无法生存而绝迹]
4.某工厂排出的废水中含有氯气,为了除去废水中的游离氯,且使废水变为中性,有人提出如图所示的方案:在废水排出管的A、B处分别注入一定量的废烧碱溶液和亚硫酸钠溶液,已知氯气和亚硫酸钠溶液的反应如下: Cl2+Na2SO3+H2O == Na2SO4+2HCl
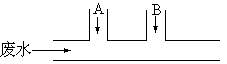 试写出:
(1)A、B处应加入的物质的化学式依次为[答:Na2SO3]和[答:NaOH]
(2) A、B处发生的反应的离子方程式是:
A[答:Cl2+SO32-+H2O
== SO42-+2H++2Cl-]
B[答:H++OH-
== H2O]
试写出:
(1)A、B处应加入的物质的化学式依次为[答:Na2SO3]和[答:NaOH]
(2) A、B处发生的反应的离子方程式是:
A[答:Cl2+SO32-+H2O
== SO42-+2H++2Cl-]
B[答:H++OH-
== H2O]
3.供选择的答案:①在水溶液中电离,并呈强酸性 ②具有高沸点、难挥发性 ③浓硫酸具有吸水性 ④浓硫酸具有脱水性 ⑤浓硫酸具有强氧化性 在下列变化中,硫酸体现的性质为: (1)铜跟浓硫酸共热,产生二氧化硫气体[答: ①⑤] (2)亚硫酸钠中加入硫酸,产生二氧化硫气体[答:①②] (3)氯化钠固体跟浓硫酸的混和物共热时产生氯化氢气体[答:②] (4)浓硫酸能用来干燥H2、O2、Cl2等,但不能用来干燥NH3、HI等[答:①③⑤] (5)纸张、布片、蔗糖等遇浓硫酸会慢慢变黑[答:④] (6)浓硫酸跟氨水反应完全后,溶液的PH值小于7[答:①] (7)蔗糖溶液中加入少量硫酸后微热,生成葡萄糖和果糖[答:①] (8)浓硫酸与溴化钠的混和物加热时产生混和气体[答:②⑤] (9)浓硫酸跟灼热的炭反应时产生混和气体[答:⑤]
2.今有A、B、C、D四种短周期元素,它们的核电荷数依次增大,A与C、B与D分别是同族元素,B、D两元素的质子数之和是A、C两元素质子数之和的两倍,这四种元素中有一种元素的单质易溶于二硫化碳,则这四种元素分别是A[答:氢]、B[答:氧]、C[答:钠]、D[答:硫] [提示:A、C也可以分别是氦、氩]
1.如果黄铜矿的成分是CuFeS2和少量的SiO2。已知S的质量百分含量为a%,则铜的质量百分含量为[答:a%];如用此矿石1吨制硫酸,矿石利用率为98%,SO2的转化率为96%,则可制得98%的硫酸[答:0.0249a]吨
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com