
题目列表(包括答案和解析)
2.下列物质中,属于纯净物的是( )
A.石油 B.液态氧 C.食醋 D.水泥砂浆
1.下列变化中,属于化学变化的是( )
A.石蜡熔化 B.汽油挥发
C.湿衣晾干 D.木柴燃烧
解:设参加反应的Ba(OH)2的质量为x
生成的BaSO4质量为:20 g+30 g-47.67 g=2.33 g ……………………(1分)
Ba(OH)2 + H2SO4= BaSO4↓+2H2O …………………………………(1分)
171 233
x 2.33 g
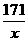 =
=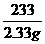 …………………………………………………………(2分)
…………………………………………………………(2分)
x=1.71 g ………………………………………………………………(1分)
Ba(OH)2的溶质质量分数=1.71 g÷25 g×100%=6.84% ………………(1分)
答:该溶液中Ba(OH)2的溶质质量分数为6.84%。
11.(共11分)(1)(每空1分,共3分)
雨水从空气中吸收了二氧化碳,生成碳酸,碳酸呈弱酸性(或:写方程式也可)
二氧化硫和氮的氧化物(或:硫的氧化物和氮的氧化物)(或:写化学式也可)
化石燃料的燃烧(或:汽车、工厂所排放的废气) (不给分:火山爆发)
(2)(实验内容及步骤4分,实验结果2分,共6分)
|
实验内容及步骤 |
应得到的实验结果 |
|
1.称取适量(如10g)大理石薄片,放入小烧杯中。 2.量取适量(如50mL pH=6.5)普通雨水,倒入步骤1小烧杯。 3.过较长时间(如一周),取出大理石片,干燥,称量剩余大理石薄片的质量。 |
大理石薄片的质量不变(如仍等于10g)。 |
|
1.称取适量(如10g)大理石薄片,放入小烧杯中。 2.量取适量(如50mL pH=3)醋酸溶液,倒入步骤1小烧杯。 3.过较长时间(如一周),取出大理石片,干燥,称量剩余大理石薄片的质量。 |
剩余大理石薄片的质量减少(如小于10g)。 |
(3)(共2分。每个0.5分。多选、错选不给分)
A、B、C、E
10.(共11分。第4小题3分,其余每空1分)
(1)NaHCO3 CuSO4 Fe
(2)物质的性质决定用途
有毒,能使人体中蛋白质失去生理活性
物质的组成和结构决定物质的性质
(3)铁是人体必需的营养元素(或:补铁;或:铁是血红素的组成成分)
(4)碳酸氢钠本身无毒;
在体内发生化学反应生成水、二氧化碳和钠盐也无毒;
钠、碳、氢、氧都是组成人体的常量元素。 (5)A
9.(共13分。每空1分)
(1)①②③④ ⑤ (2) ② ④
根据反应物和生成物的种类和类别(或:根据反应物和生成物的种类和组成)
(3) H2和O2 Zn+H2SO4=ZnSO4+H2↑ H+ 和Zn
锌原子失去电子,变成锌离子,氢离子得到电子变成氢原子,两个氢原子结合生成一个氢分子。 H+、OH- 不相同
③是化学变化,原子核(元素和原子的种类)不变;⑥是核变化,原子核(元素和原子的种类)发生改变。
(4)②
8.(共8分。方程式每个1分,其余每空一分)
(1)A (2)D (3)A C
 (4)CaCO3 CaO+CO2↑
(4)CaCO3 CaO+CO2↑
CaO+H2O=Ca(OH)2
Ca(OH)2+2HCl=CaCl2+2H2O
 C2H5OH+3O2 2CO2+3H2O
C2H5OH+3O2 2CO2+3H2O
1. C 2. B 3. A 4. C 5. D 6. D 7. A
第Ⅱ卷 (非选择题 共49分)
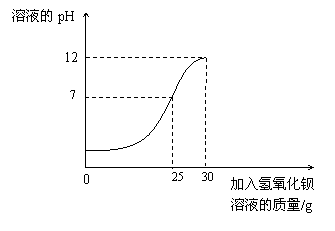
12.(6分)为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20 g,逐滴加入氢氧化钡溶液30 g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示)。过滤后得滤液47.67 g。请你通过计算,求出氢氧化钡溶液的溶质质量分数。可能用到的相对原子质量:H-1 O-16 S-32 Ba-137
11.(11分)化学与环境保护--探究酸雨的腐蚀性
我国道教发源地山东威海圣经山摩崖石刻,为国内罕见的大型道教石刻,可称为瑰宝。圣经山摩崖石刻的材质是大理石,主要成分是碳酸钙,现在字迹已模糊不清。摩崖石刻被腐蚀,是否是酸雨所致?试回答下列问题:
(1)酸雨的成因:即使大气没有受到污染,正常的雨水或河水也呈微弱酸性(pH在5.6-7之间),原因是 。酸雨的酸性比正常雨水强,是因为雨水吸收了被污染的大气中的 等有害气体。大气中这些有害气体主要来自于 。
(2)定量实验探究:
查阅资料及定性实验表明:(1)醋酸和酸雨的酸性程度差不多,pH在5.6-3之间;(2)酸雨(醋酸)确实能加重大理石腐蚀的程度。(3)定性实验显示:将大理石放入pH=3的醋酸溶液中,短时间内几乎看不出有气泡产生。
现提供下列仪器和试剂:
仪器:烧杯、托盘天平、镊子、量筒、胶头滴管。
药品:pH=6.5的普通雨水、pH=3醋酸溶液、大理石薄片。
请你设计一个“定量实验方案”,证明摩崖石刻被腐蚀,主要与酸雨有关,与普通雨水无关。
|
实验内容及步骤 |
应得到的实验结果 |
|
|
|
(3)下列与保护摩崖石刻有关的说法中,你同意的是( )
A.了解哪种人类活动最容易引起酸雨
B.引起酸雨原因的结论应建立在科学研究的基础上
C.保护摩崖石刻要建立在有关损坏原因的科学证据的基础上
D.要从根本上预防酸雨的危害,应禁止工厂和汽车排放气体
E.要减少酸雨的危害,应研究和推广减少有害气体排放的技术
F.要从根本上保护摩崖石刻,主要应研究修复被酸雨损伤的摩崖石刻的方法与技术
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com