
题目列表(包括答案和解析)
12.叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是 ( )
A HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3)>c(OH)
B HN3与NH3作用生成的叠氮酸铵是共价化合物
C NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-)>c(OH-)>c(H+)
D N3-与CO2含相等电子数
11、在试管中注入某红色溶液,给试管加热,溶液颜色逐渐变浅,则原溶液可能是:
①滴有石蕊的CO2溶液 ②滴有石蕊的NH4Cl溶液 ③滴有石蕊的H2SO4溶液
④滴有酚酞的氨水溶液 ⑤滴有酚酞的氢氧化钠溶液 ⑥滴有酚酞的饱和氢氧化钙溶液
⑦滴有酚酞的Na2CO3溶液 ⑧Fe (SCN)3溶液 ⑨溶有SO2的品红溶液
A、①④⑥ B、③⑤⑦⑧ C、④⑥ D、②④⑥⑨
10.t℃时,将一定质量的某物质的不饱和溶液均分为三份,分别加热蒸发溶液,然后把温度降至t℃,已知从三份溶液中蒸发的溶剂质量分别为10g、20g、30g,析出晶体(不含结晶水)质量分别为a、b、c(单位g,且a、b、c均大于零),则a、b、 c三者的关系为 ( )
A、c=2b-a B、c=a+b C、c=a+2b D、c=2a+b
9.将3mol A 和2.5mol B 充入容积为2L的密闭容器中,发生如下反应:
3A(气) + B(气) 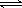 nC(气) + 2D(气),经测定,5min后反应达平衡状态,生成1mol D,
v(C)=0.1 mol·L-1·min-1 ,下列结论中错误的是
( )
nC(气) + 2D(气),经测定,5min后反应达平衡状态,生成1mol D,
v(C)=0.1 mol·L-1·min-1 ,下列结论中错误的是
( )
① 平衡时B的转化率为20% ② 平衡时B的浓度为1mol·L-1
③ 经计算,n值为1 ④ v(A) = 0.3 mol·L-1·min-1
(A) ①、② (B) ①、④ (C) ②、③ (D) ③、④
8.下列关于卤素的叙述中正确的是 ( )
①卤素的钾盐中,最易被氧化的氟化钾:②溴中溶有少量氯气,可以用加入溴
化钠再用汽油萃取的方法提纯;③溴化银具有感光性,碘化银不具感光性;④某溶液与淀粉碘化钾溶液反应出现蓝色,则证明该溶液是氯水或溴水;⑤氟气跟氯化钠水溶液反应,一定有HF和O2生成;⑥氯气跟水反应时,水既不是氧化剂也不是还原剂。
(A)①③⑤ (B)②④⑥ (C)②⑤⑥ (D)①③④
7. 下列各组物质的类别归属正确的是 ( )
A. 同位素: 1H2、2H2、3H2 B. 非电解质:Cl2、BaSO4、C2H5OH
C. 分子晶体: I2、SO3、固态氩 D. 纯净物: 重水、双氧水、矿泉水
6. 已知氯化铁溶液中通入硫化氢可发生反应:2FeCl3+H2S→2FeCl2+S↓+2HCl。在标准状况下,向100mLFeCl3溶液中通入a L的H2S气体恰好反应后,再加入足量的铁粉充分反应。所得溶液经测定金属阳离子的浓度为3mol/L,若反应过程中溶液体积不变,则原FeCl3溶液的物质的量浓度为( )
A.1.5mol/L B.1 mol/L C.2 mol/L D.无法确定
5.X、Y均为周期表中短周期元素,X原子的最外层电子数是Y原子的最外层电子数的6倍,它们能彼此形成的化合物可以满足2个或8个电子的稳定结构,下列说法不正确的是 ( )
A.X、Y形成的化合物的分子式一定为Y2X
B.X与Y形成的化合物可能具有强氧化性
C.X可能在第三周期,Y在第二周期
D. X、Y形成的化合物可能使溴水褪色
4.以下实验装置一般不用于分离物质的是 ( )
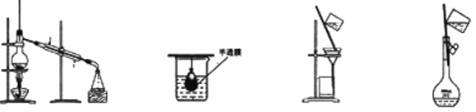
A B C D
3.设阿伏加德常数为NA。则下列说法正确的是 ( )
A 常温常压下,11.2L甲烷中含有的氢原子数为2NA
B 标准状况下,0.3mol二氧化硫中含有氧原子数为0.3NA
C 常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA
D 常温下,1L 0.1mol/L MgCl2溶液中含Mg2+数为0.2NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com