
题目列表(包括答案和解析)
20.(8分)CO、C2H4均为常见的可燃性气体。
(1)等体积的CO和C2H4在相同条件下分别完全燃烧,转移的电子数之比是
(2)120℃、101 kPa下,a mL由CO、C2H4组成的混合气体在b mL O2中完全燃烧后,恢复到原温度和压强。
① 若混合气体与O2恰好完全反应,则混合气体中C2H4的体积为 mL(用含a、b的式子表示)。
② 若燃烧后气体体积缩小了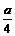 mL,则混合气体中CO的体积为
mL,a与b
mL,则混合气体中CO的体积为
mL,a与b
关系的数学表示式是 。
19.(14分)聚合硫酸铁(PFS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铁的氧化物为原料来制取聚合硫酸铁,实验步骤如下:
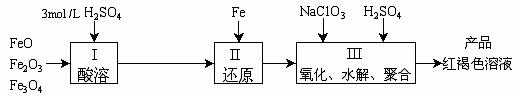
(1)用98%的硫酸配制3mol /L的硫酸,所需的玻璃仪器除量筒、烧杯、玻璃棒外,还有 。
(a)容量瓶 (b)胶头滴管 (c)烧瓶
(2)用NaClO3氧化时反应方程式如下:
6FeSO4+NaClO3+3H2SO4 =3Fe2(SO4)3+NaCl+3H2O
若改用HNO3氧化,则反应方程式如下:
6FeSO4+2HNO3+3H2SO4 =3Fe2(SO4)3+2NO↑+4H2O
已知1 mol HNO3价格0.16元、1 mol NaClO3价格0.45元,评价用HNO3代替NaClO3作氧化剂的利弊,利是 ,弊是 。
聚合硫酸铁溶液中 与Fe3+ 物质的量之比不是3︰2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中
与Fe3+ 物质的量之比不是3︰2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中 与Fe3+物质的量之比。
与Fe3+物质的量之比。
(3)测定时所需的试剂 。
(a)NaOH (b)FeSO4 (c)BaCl2 (d)NaClO3
(4)需要测定 和 的质量(填写化合物的化学式)。
(5)选出测定过程中所需的基本操作(按操作先后顺序列出) 。
(a)萃取、分液 (b)过滤、洗涤 (c)蒸发、结晶
(d)冷却、称量 (e)烘干或灼烧
18.(14分)A、B、C、D、E、F、G、X、Y和M等物质有如图转化关系,其中M为黑色粉末,X、Y为常见的气体单质,D、G为常见金属单质。上述各步转化中只写出其中一种生成物,其他生成物没有写出(也可能反应 只有一种生成物)。
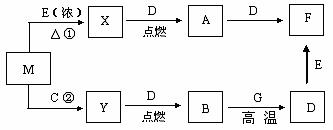
(1)写出有关物质化学式:M ,X ,C 。
(2)指出M在相关反应中的作用:反应①中是 剂,反应②中是 剂。
(3)写出A→F离子方程式 。
(4)写出B→D化学方程式 。
17.(11分)X、Y、Z、W为按原子序数由小到大排列的四种短周期元素。
已知:①X可分别与Y、W形成X2Y,X2Y2、XW等共价化合物;
②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。
请回答:
(1)Z2Y的化学式是 。
(2)w的元素符号是 ,它的原子结构示意图为 。
(3)Z2Y2与X2Y反应的化学方程式是 。
(4)铜屑放入稀硫酸不发生反应,若在稀硫酸中加入X2Y2,铜屑可逐渐溶解,该反应的离子方程式是 。
16.(8分)通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
|
化学键 |
Si-O |
Si-Cl |
H-H |
H-Cl |
Si-Si |
Si-C |
|
键能 / kJ·mol-1 |
460 |
360 |
436 |
431 |
176 |
347 |
请回答下列问题:YCY
(1)比较下列两组物质的熔点高低(填“>”或“<”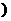
SiC______Si;SiCl4_________Si
(2)已知工业上高纯硅(1molSi中含2mol硅-硅键)通常用SiCl4(g)与H2反应制备,写出该反应的热化学方程式__ ____
15.一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g) 3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是 ( )
3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是 ( )
A.2 mol C
B.2 mol A 3mol B和1 mol He(不参加反应)
C.1 mol B和1 mol C
D.2 mol A 3 mol B和3 mol C
第二卷(非选择题 共55分)
本试卷包括5小题
14.下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
|
|
|
||
|
X |
|
|
|
|
W |
Y |
|
R |
|
|
|
Z |
|
A.常压下五种元素的单质中Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.Y元素的非金属性比W元素的非金属性强
D.W的氢化物沸点比X的氢化物的沸点高
13.下列叙述正确的是 ( )
A.铜锌原电池中铜为负极
B.0.1 mol N2与0.1 mol H2在一定条件下反应达到平衡时,生成0.2 mol氨
C.18 g H2O中含1 mol氧原子
D.1 mol·L-1 AlCl3溶液中,铝离子物质的量浓度为1 mol·L-1
12.有下列四组物质,如果把某组物质中的后者逐滴加入到前者中至过量,将出现“先产生白色沉淀,后白色沉淀溶解”的现象,这组物质是 ( )
A.氯化钠溶液、硝酸银溶液 B.硫酸亚铁溶液、氢氧化钠溶液
C.氯化铝溶液、浓氨水 D.偏铝酸钠溶液、稀硫酸
11.pH=a的某电解质稀溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH>a,则该电解质可能是 ( )
A.NaOH YCY B.H2SO4 C.AgNO3 D.Na2SO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com