
题目列表(包括答案和解析)
20.(8分)(1)某学生的实验报告中有下列数据:
①用托盘天平称取11.7 g氯化钠; ②用100 mL的量筒量取21.48 mL盐酸;
③用容量瓶配制480 mL 1 mol/L的氯化钠溶液;
④用酸式滴定管量取25.00 mL硫酸溶液;
⑤用pH试纸测定H2SO4溶液的pH为3.2。其中合理的是
A.只有①④ B.只有②④ C.只有①③ D.只有②⑤
(2)向鸡蛋白水溶液中加入少量的 (填一种试剂),再 (填实验操作名称)可得到较纯的鸡蛋白固体
(3)鉴别苯、苯酚、1-己烯、四氯化碳、碘化钠溶液,应选用的试剂是
19. 向2mL 0.5mol·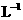 的
的 溶液中加入3mL 5mol·
溶液中加入3mL 5mol·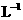 KF溶液,发现
KF溶液,发现 溶液渐渐褪至无色,再加入KI溶液和
溶液渐渐褪至无色,再加入KI溶液和 振荡后,静置,不见
振荡后,静置,不见 层有紫红色,则下列说法正确的是( )
层有紫红色,则下列说法正确的是( )
A. 不与
不与 发生反应 B.
发生反应 B. 与
与 结合成不与
结合成不与 反应的物质
反应的物质
C.F-使 的还原性减弱 D.
的还原性减弱 D. 被F-还原为
被F-还原为 ,使溶液中不再存在
,使溶液中不再存在
18.以M原子为中心形成的MX2Y2分子中,X、Y分别只以单键与M结合,
下列说法正确的是
A.若MX2Y2分子为平面四边形则无同分异构体
B.若MX2Y2分子为平面四边形就有两种同分异构体
C.若MX2Y2分子为四面体形则无同分异构体
D.若MX2Y2分子为四面体形就有两种同分异构体
17. 不能反映反应2A(g)+B(g) 2C(g) ; △H<0 的有关变化的图象是( )
2C(g) ; △H<0 的有关变化的图象是( )

16.向1 mol赤热的Cu2S通入足量水蒸气,生成2 mol H2,则Cu2S应转化成
A.Cu和SO2 B.Cu和S C.CuO和SO2 D.CuO和S
15.下列溶液中各离子浓度的大小顺序正确的是
A.0.1 mol∙L-1的NH4Cl溶液与0.05 mol∙L-1NaOH溶液等体积混合
c(Cl-)> c(NH4+)>c(Na+)>c(OH-)> c(H+)
B.0.2 mol∙L-1 Na2CO3溶液 c(OH-)=c(HCO3-)+ c(H+)+2c(H2CO3)
C.0.1 mol∙L-1的(NH4)2SO4溶液 c(SO42-)>c(NH4+)> c(H+)>c(OH-)
D.0.2 mol∙L-1 NaHCO3溶液 c(Na+)> c(HCO3-)> c(CO32-)>c(OH-)
14. 将物质的量相等的硫酸铝和硫酸铵溶于水形成V mL混合溶液,向混合溶液中逐滴加入某氢氧化钠的溶液(其物质的量浓度为混合液中两溶质的物质的量浓度之和),直至过量。下列表示氢氧化钠溶液加入的体积(x)与溶液中沉淀物的物质的量(y)的关系示意图正确的是
将物质的量相等的硫酸铝和硫酸铵溶于水形成V mL混合溶液,向混合溶液中逐滴加入某氢氧化钠的溶液(其物质的量浓度为混合液中两溶质的物质的量浓度之和),直至过量。下列表示氢氧化钠溶液加入的体积(x)与溶液中沉淀物的物质的量(y)的关系示意图正确的是



13.元素X、Y在周期表中处于相邻周期,这两种元素原子的核电荷数之和为21,Y原子核外电子数比X原子核外电子数多5,则下列叙述中正确的是
A.Y单质在空气中可以燃烧生成含YX元素的化合物
B.氢元素与X、Y三种元素组成的化合物在水中存在着两种电离方式
C.含Y与X 两种元素组成的阴离子的溶液,与酸反应时,实验操作顺序不同实验现象也不相同
D.Y与强酸或强碱溶液反应时,都生成Y的阳离子
12.已知在酸性条件下有反应,2Cu+═Cu2+ + Cu 氢气还原氧化铜实验由于反应温度不同,可能产生Cu或Cu2O 。某学生对某次氢气还原氧化铜实验产物做了如下实验,实验操作和实验现象列表如下:
|
加入试剂 |
稀硫酸 |
浓硫酸并加热 |
稀硝酸 |
浓硝酸 |
|
实验现象 |
红色固体 蓝色溶液 |
无色气体 |
无色气体 蓝色溶液 |
红棕色气体 蓝色溶液 |
由此推出本次氢气还原氧化铜实验产物
A.是Cu B.是Cu2O
C.一定有Cu,可能有Cu2O D.一定有Cu2O,可能有Cu
11. 第VA族元素的原子(以R表示)与A原子结合形成RA3气态分子,其空间构型呈三角锥形。PCl5 在气态和液态时,分子结构如图所示,下列关于PCl5 分子的说法中不正确的是
第VA族元素的原子(以R表示)与A原子结合形成RA3气态分子,其空间构型呈三角锥形。PCl5 在气态和液态时,分子结构如图所示,下列关于PCl5 分子的说法中不正确的是
A.每个原子都达到 8 电子稳定结构
B.键角(∠ClPCl)有90o、120o、180o几种
C.PCl5 受热后会分解生成分子空间构型
呈三角锥形的 PCl3
D.分子中5个P-Cl 键键能不都相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com