
题目列表(包括答案和解析)
1.机床的废切削液中含有2%~5%的亚硝酸钠,直接排放会造成环境污染,为使其能除去NO2-‑,并且不引起第二次污染出现,应选用的试剂是
A.HNO3 B.NH4Cl C.FeSO4 D.浓H2SO4
30.(11分)实验室常用燃烧分析法来测定有机物中碳和氢的质量分数,这种方法是用氧化铜作催化剂,在750℃时,用氧气流将样品氧化成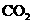 和
和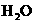 ,再根据
,再根据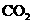 和
和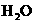 的质量求出有机物中碳和氢的质量分数.现用下列各仪器装置来确定乙炔分子中碳、氢两种元素的质量比.
的质量求出有机物中碳和氢的质量分数.现用下列各仪器装置来确定乙炔分子中碳、氢两种元素的质量比.
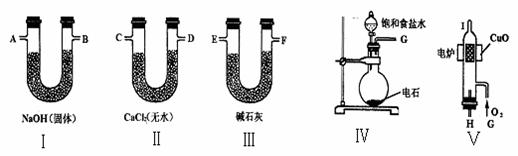
回答下列问题:
(1)若产生的气体由左向右流向,各装置导管的连接顺序是:________接________、________接________、________接________、________接 A
(2)装置Ⅰ的作用是___________________________;
装置Ⅱ的作用是________________________________;
装置Ⅲ的作用是_________________________________.
(3)装置Ⅳ中的化学方程式________________________________;装置Ⅴ中的化学方程式______________________________________.
(4)实验前称得Ⅰ、Ⅱ两装置的质量分别变为 和
和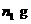 ,实验完毕,称得Ⅰ、Ⅱ两装置的质量分别变为
,实验完毕,称得Ⅰ、Ⅱ两装置的质量分别变为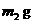 和
和 ,则乙炔分子中碳原子
,则乙炔分子中碳原子
和氢原子的原子个数比为___________________________
(列出算式才能得分).
29、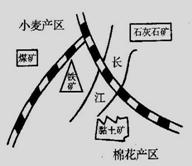 (5分)长江中下游某地探明有一座大型磁铁矿,该铁矿附近有炼焦用的烟煤矿,石灰石矿,附近山冈上盛产黏土,如右图。运用有关知识回答下列问题:
(5分)长江中下游某地探明有一座大型磁铁矿,该铁矿附近有炼焦用的烟煤矿,石灰石矿,附近山冈上盛产黏土,如右图。运用有关知识回答下列问题:
⑴根据上述资源和矿产,你认为当地的工业“龙头” 是 。
A、能源工业 B、钢铁工业
C、化肥工业 D、有机化工
⑵如果当地发展上述工业,则还需建造与之配套的工厂是 _ 。
A、炼焦厂 B、火力发电厂 C、硫酸厂 D、陶瓷厂
⑶为了充分利用资源与龙头工业密切联系,你认为该地区还可建造的工厂是 ____ 。
A、重型机械厂 B、水泥厂 C、化肥厂 D、造船厂
28.(10分)某化学课外小组设计了如下图所示的实验装置,进行气体性质实验.图中箭头表示气体流向.A表示一种纯净、干燥的气体,B是另一种气体,反应进行一段时间后,装置已中有红棕色气体生成.实验
中所用的药品和干燥剂只能从下列物质中选取: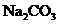 、
、 、
、 、
、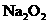 、NaCl、无水
、NaCl、无水 、
、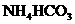 、碱石灰等固体和
、碱石灰等固体和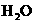 、蒸馏水.
、蒸馏水.

根据图中装置和反应现象请回答:
(1)丁中的干燥剂应选 ________,不选另一种干燥剂的理由是_____
____________________________________________________.
(2)甲中发生反应的化学方程式为______________________________
(3)戊中发生的主要反应的化学方程式为_______________________,此反应是(吸热、放热)________反应,
(4)当已中充满红棕色气体后,停止给丙加热,并关闭a、b两个活塞,若将已浸入冰水中,则已中会出现的现象是_______________,简述产生此现象的原因_______________________________________
___________________________________________________.
27. (10分)由于Fe (OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe (OH)2沉淀,应用下图电解实验可以制得白色的纯净的Fe (OH)2沉淀。两电极材料分别为石墨和铁。
(10分)由于Fe (OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe (OH)2沉淀,应用下图电解实验可以制得白色的纯净的Fe (OH)2沉淀。两电极材料分别为石墨和铁。
⑴ 阳极材料应为__________,






 电极反应式为_________________________。
电极反应式为_________________________。
⑵ 电解液C可以是__________。
A.纯净水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
⑶ d为苯,其作用是____________________________,在加入苯之前对C应作何简单处理________________
⑷ 为了在较短时间内看到白色沉淀,可采取的措施是________。
A.改用稀硫酸作电解液 B.适当增大电源的电压。
C.适当减小两电极间距离 D.适当降低电解液的温度。
⑸ 若C中用Na2SO4溶液,当电解一段时间看到白色Fe (OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,混合物中另一明显现象为__________________________________________________________。
26.(9分)一种澄清透明的溶液中可能含有下列离子:K+、Fe3+、Ba2+、Al3+、NH4+、Cl-、NO3-、HCO3-、SO42-现做以下实验:
(1)将溶液滴在蓝色石蕊试纸上,试纸呈红色
(2)取少量溶液,加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀
(3)将(2)中的沉淀过滤。由滤液中加入硝酸银溶液产生白色沉淀
(4)另取溶液,逐滴加入氢氧化钠溶液至过量,观察到有棕色沉淀生成,且沉淀量有部分减少。由此可以推断:
①溶液中肯定存在的离子有: 。
②溶液中肯定不存在的离子有:________________________。
③溶液中还不可能确定是否存在的离子有: 。
25、(7分)硫酸是基础化学工业的重要产品和原料原料。硫酸在下列用途或反应中各表现的性质是:A、高沸点 B、强酸性 C、吸水性 D、脱水性 E、强氧化性 F、催化作用 (提示:可能有重复多个选项)
⑴实验室制取氯化氢气体(固体氯化钠和浓硫酸共热) ;
⑵实验室制乙烯 __ ;
⑶可用作某些气体的干燥剂 ___ ;
⑷铝制品容器可以盛放浓硫酸 ___ ;
⑸与乙醇和乙酸共热制取乙酸乙酯 ___ ;
⑹清洗镀件 ___ ;
⑺浓硫酸能使湿润的蓝色石蕊试纸先变红后变黑 ____ 。
第 II卷(非选择题共52分)
24、
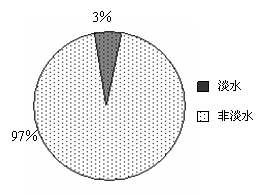 观察右图,若用1 L水来代表地球上的总水量,要比较精确地量取地球上的淡水量,应选择的仪器是
观察右图,若用1 L水来代表地球上的总水量,要比较精确地量取地球上的淡水量,应选择的仪器是
A. 100 mL烧杯
B. 50 mL烧杯
C. 100 mL量筒
D. 50 mL量筒
|
化 学 试 卷
班次 姓名 座号 得分
23.下列实验操作与安全事故处理错误的是
A. 使用水银温度计测量烧杯中水浴温度时,不慎打破水银球,用滴管将水银吸出放入水封的小瓶中,残渣的温度计插入装有硫粉的广口瓶中
B. 用试管夹从试管底由下往上夹住距试管口约 处,手持试管夹长柄末端,进行加热
处,手持试管夹长柄末端,进行加热
C. 制备乙酸乙酯时,将乙醇和乙酸依次加入到浓硫酸中
D. 把玻管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻管插入端,缓慢旋进孔中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com