
题目列表(包括答案和解析)
10.25℃时,0.1mol·L-1的某一元碱MOH溶液pH = 13,将它和某一元酸HA的溶液等体积混合,混合后的溶液恰好为中性。下列判断正确的是
A.HA溶液的pH一定为1 B.盐MA可能水解
C.HA物质的量浓度一定为0.1mol·L-1
D.混合后溶液中,c(M+)一定等于c(A-)
9.向一种溶液中滴加另一种溶液后,溶液的颜色不发生变化的是
A.碳酸钠溶液中滴加稀硫酸 B.氯化铁溶液中滴加硫氰化钾溶液
C.碘水中滴加淀粉碘化钾溶液 D.酸性高锰酸钾溶液中滴加亚硫酸钠溶液
8.常温下,测得某无色溶液中由水电离出的C(H+) = 1×10-13 mol·L-1,则该溶液中一定能共存的离子组是
A.AlO2-、NO3-、Na+、Cl- B.Mg2+、SO42-、Na+、ClO-
C.Fe3+、NO3-、K+、SO42- D.Ba2+、K+、NO3-、Cl-
7.下列离子方程式中,正确的是
A.在氯化亚铁溶液中通入氯气:Fe2+ + Cl2 = Fe3+ + 2Cl-
B.三氯化铁溶液跟过量氨水反应:Fe3+ + 3NH3·H2O = Fe(OH)3↓+ 3NH4+
C.碳酸氢钙溶液跟稀硝酸反应:Ca(HCO3)2 + 2H+ = Ca2+ + 2H2O + 2CO2↑
D.偏铝酸钠的水溶液显碱性:AlO2- + 2H2O
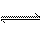 Al(OH)3↓+ OH-
Al(OH)3↓+ OH-
6.阿佛加德罗常数约为6.02×1023·mol-1,下列说法中正确的是
A.标准状况下,1.12L的SO3所含的原子数约为0.2×6.02×1023
B.1 mol MgCl2中含有的离子数约为2×6.02×1023
C.1.8g的NH4+离子中含有的电子数约为6.02×1023
D.2.4g金属镁变为镁离子时失去的电子数约为0.1×6.02×1023
5.下列实验方案合理的是
A.用饱和碳酸钠溶液除去乙酸乙酯中混有的乙酸、乙醇杂质
B.用加入浓溴水的方法分离甲苯和苯酚的混合液
C.用点燃的方法来除去二氧化碳中混有的少量一氧化碳
D.用过滤的方法除去苯酚中的三溴苯酚
4.已知H2(g) + Cl2(g) = 2HCl(g);△H = -184.6 kJ·mol-1 ,则反应HCl(g) = H2(g) + Cl2(g)的△H为
A. + 184.6 kJ·mol-1 B.- 92.3 kJ·mol-1
C.+ 92.3 kJ·mol-1 D.- 369.2 kJ·mol-1
3.近代化学常用CaH2作生氢剂,其化学方程式为:CaH2 + 2H2O = Ca(OH)2 + 2H2↑,其中水的作用是
A.氧化剂 B.还原剂 C.溶剂 D.既是氧化剂又是还原剂
2.下列关于某些社会热点问题的说法中,不正确的是
A.光化学烟雾的产生与碳氢化合物、氮氧化合物的排放有关
B.禁止使用含铅汽油是为了提高汽油的燃烧率
C.臭氧空洞的形成与氟氯烃或氮氧化物的泄漏到大气中有关
D.甲醛是某些劣质装饰板材释放的常见污染物之一
1.下列物质属于天然高分子化合物的是
A.聚氯乙烯 B.尼龙 C.油脂 D.纤维素
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com