
题目列表(包括答案和解析)
20.(10分)发射航天火箭常用氮的氢化物肼(N2H4)作燃料。试回答下列有关问题:
⑴ 写出N2的电子式________________
⑵ 液态NH3类似H2O,也能微弱电离且产生电子数相同的两种离子,则液态NH3电离方程式为________________________
⑶ 25℃时,0.1 mol·L-1 NH4NO3溶液中水的电离程度___________(填“大于”、“等于”或“小于”)0.1 mol·L-1 NaOH水溶液中水的电离程度。若将0.1 mol·L-1 NaOH和0.2 mol·L-1 NH4NO3两溶液等体积混合,所得溶液中离子浓度由大到小的顺序为__________________________________。
⑷ 在结构上N2H4和NH3的关系有如H2O2和H2O的关系。N2H4能发生下列反应:
N2H4 + H3O+
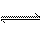 N2H5+ +
H2O
N2H4 + H2O
N2H5+ +
H2O
N2H4 + H2O  N2H5+ + OH-
N2H5+ + OH-
N2H5+ + H2O  N2H62+ + OH- N2H5+
+ H2O
N2H62+ + OH- N2H5+
+ H2O  N2H4 + H3O+
N2H4 + H3O+
据此可得出的结论是_______________
A.肼水解显酸性 B.肼在水中电离出H+离子
C.肼是二元弱碱 D.肼是二元弱酸
⑸ 完成下列反应方程式并配平:
__NH3 + ___NaClO == ___NaCl + ___N2H4 + ___ ___________
⑹ 发射火箭时肼(N2H4)为燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知4 gN2H4(g)上述反应中放出71kJ的热量,写出该反应的热化学方程式
___________________________________________________________
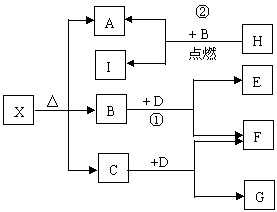
19.(9分)已知X是一种盐,H是常见金属单质,
F、I是常见非金属单质,E、G都是工业上重
要的碱性物质,它们有右图所示的关系。
试回答下列问题:
⑴ G的化学式为______________
⑵ 写出下列反应的化学方程式
① ___________________________
② ___________________________
⑶ X在医药上用作解酸剂,与盐酸作用时,生成B的物质的量与消耗盐酸的物质的量之比为3 : 8,则X的化学式为_____________;X与盐酸反应的化学方程式为____________________________。
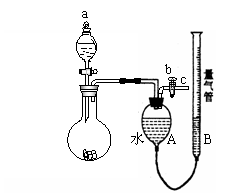
18.(15分)某校课外实验小组同学设计了如图所示的实验装置进行实验(夹持装置已略去)。
⑴ 该小组同学用该装置进行“乙炔的制取及其燃烧性质的验证”实验。① 仪器a的名称是____________,实验开始时使用该仪器的操作方法是______________________。
② 点燃乙炔前,需要验纯。简述验纯的操作方法:_______________________。
③ 在导管口c处点燃乙炔,观察到的现象是______________________________。
⑵ 该装置还可用于制取并收集少量其他气体。请帮助该小组同学完成下表。
|
制取气体 |
药品 |
化学方程式 |
|
O2 |
_______、_________ |
_____________________ |
|
____ |
NaOH浓溶液、Al |
_____________________ |
⑶ 某同学用该装置进行实验,确定某饱和醇的结构。反应前,先对量气管进行第一次读数;反应后,待装置温度冷却到室温,再对量气装置进行第二次读数(表中读数已折合成标准状况下的数值)。实验数值如下:
|
|
饱和醇的质量 |
金属钠的质量 |
量气管第一次读数 |
量气管第二次读数 |
|
① |
0.62 g |
5.0 g(足量) |
40 mL |
264 mL |
|
② |
0.31 g |
2.5 g (足量) |
40 mL |
152 mL |
已知该饱和醇的相对分子质量为62。根据上述数据可确定该饱和醇的结构式为______________ 。
17.(7分)在足量的稀氯化亚铁溶液中,加入1-2滴液溴,振荡后溶液变为黄色。
⑴ 甲同学认为这不是发生化学反应所致,使溶液变黄色的物质是:___________(填粒子的化学式,下同);乙同学认为这是发生化学反应所致,使溶液变黄色的物质是__________。
⑵ 现提供以下试剂:
A.酸性高锰酸钾 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液
根据所学知识判断,________同学(填甲或乙)的推断是正确的。用两种方法加以验证,写出选用的试剂编号及实验中观察到的现象:
|
|
选用试剂 |
实验现象 |
|
第一种方法 |
|
|
|
第二种方法 |
|
|
16.含8.0gNaOH的溶液中通入一定量H2S后,将得到的溶液低温小心蒸干,称得无水物7.9g,则该无水物中一定含有的物质是
A.Na2S B.NaHS C.Na2S和NaHS D.NaOH和NaHS
15.在一密闭容器中通入A、B两种气体,一定条件下发生如下反应:
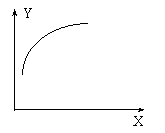 2A(g) + B(g)
2A(g) + B(g)  2C(g)
; △H < 0 达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是
2C(g)
; △H < 0 达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是
|
|
X |
Y |
|
A |
再加入A |
B的转化率 |
|
B |
再加入C |
A的体积分数 |
|
C |
缩小体积 |
A的转化率 |
|
D |
升高温度 |
 混合气体密度 混合气体密度 |
14.2006年3月2日英国《泰晤士报》报道指出:汽水 中如果同时含有苯甲酸钠(防腐剂,C6H5COONa)与维生素C(抗氧化剂,结构式如图)可能会相互作用生成苯。下列说法不正确的是
A.苯是非极性分子
B.苯在一定条件下能发生取代反应和加成反应
 C.维生素C在碱性溶液中能稳定存在
C.维生素C在碱性溶液中能稳定存在
D.维生素C可溶于水
13.下列叙述正确的是
A.分子晶体中都存在共价键
B.F2、Cl2、Br2、I2的熔沸点逐渐升高与分子间作用力有关
C.含有极性共价键的化合物分子一定不含非极性键
D.只要是离子化合物,其熔点一定比共价化合物的熔点高
12.如图:一种微型钮扣电池,其电极材料分别为Ag2O和Zn,电解质溶液是KOH溶液。负极的反应式为:Zn - 2e- + 2OH- = ZnO + H2O,该电池总反应式为:Zn + Ag2O = ZnO + 2Ag。根据以上提供的资料,判断下列说法正确的是
A.正极的反应式为:Ag2O + 2e- + H2O = 2Ag + 2OH-
B.放电时负极附近溶液的pH不变
C.放电时每消耗6.5gZn,转移电子0.1mol
D.放电时溶液中阴离子向正极方向移动,阳离子向负极方向移动
11.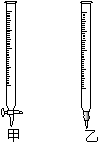 用已知物质的量浓度的NaOH溶液测定某H2SO4溶液的浓度,滴定管如图甲、乙所示。从下表中选出的正确的是组合是
用已知物质的量浓度的NaOH溶液测定某H2SO4溶液的浓度,滴定管如图甲、乙所示。从下表中选出的正确的是组合是
|
|
锥型瓶中溶液 |
滴定管中溶液 |
选用指示剂 |
选用滴定管 |
|
A |
碱 |
酸 |
石蕊 |
乙 |
|
B |
酸 |
碱 |
酚酞 |
甲 |
|
C |
碱 |
酸 |
甲基橙 |
甲 |
|
D |
酸 |
碱 |
酚酞 |
乙 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com