
题目列表(包括答案和解析)
15.实验室制备硝酸铝[Al(NO3)3·9H2O]可使用下列方法:
 。
。
反映上述有关反应的离子方程式错误的是( )
A.2Al+2OH-+2H2O=2AlO2-+3H2↑ B.2HCO3-+2AlO2-+H2O=2CO2↑+2Al(OH)3↓
C.NH4++AlO2-+2H2O=NH3·H2O+ Al(OH)3↓ D.3H++Al(OH)3===Al3++3H2O
14.相同溶质的两份溶液,一份质量分数为ω1,密度为ρ1g·cm-3,浓度为amol·L-1,另一份质量分数为ω2,密度为 ρ2g·cm-3,浓度为bmol·L-1,若2a=b,
ω2<2ω1,则ρ1与ρ2的大小关系是( )
A.ρ1=ρ2 B.ρ1>ρ2 C.ρ1<ρ2 D.无法比较
13.下列离子方程式正确的是
A、在碳酸氢钙溶液中加入过量的氢氧化钠溶液
Ca2++2HCO3-+2OH- === CaCO3↓+2H20+CO32-
B、在溴化亚铁溶液中通入过量的Cl2气
Fe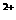 +2Br
+2Br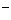 +2Cl2===Fe
+2Cl2===Fe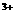 +Br2+4Cl
+Br2+4Cl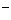
C、在硫酸溶液中加入氢氧化钡溶液至溶液恰好呈中性
H+ +SO42-+OH-+Ba2+===BaSO4↓+H2O
D、在次氯酸钙溶液中通入二氧化硫至过量
Ca2+ +2ClO-+H2O + SO2==CaSO3↓+2HClO
12.右图中a、b、c、d、e为周期表前4周期的一部分,下列叙述正确的是
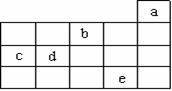
A.b元素除0价外,只有一种化合价
B.五种元素中,c元素形成的单质性质最稳定
C.c、d元素最高价氧化物的水化物酸性:c > d
D.e元素在自然界中主要存在于海水中
11.已知a、b、c、d、e分别是Ca(OH)2、Ca(HCO3)2、HCl、Ba(NO3)2、Na2CO3五种物质水溶液中的一种,它们相互反应情况如下:
|
注:“↓”表示生成沉淀 “↑”表示生成气体 “-”表示无明显现象 |
|
|
a |
b |
c |
d |
e |
|
c |
↓ |
↓ |
/ |
↑ |
- |
|
b |
↓ |
/ |
↓ |
- |
- |
可以判断c与e分别为( )
A.Ca(HCO3)2与Ba(NO3)2 B.Ca(OH)2与Ba(NO3)2
C.Na2CO3与Ca(HCO3)2 D.HCl与Ca(OH)2
10.下列关于氧化物的各项叙述正确的是:①酸性氧化物肯定是非金属氧化物 ②非金属氧化物肯定是酸性氧化物 ③碱性氧化物肯定是金属氧化物 ④金属氧化物都是碱性氧化物 ⑤酸性氧化物均可与水反应生成相应的酸 ⑥与水反应生成酸的氧化物不一定是酸酐,与水反应生成碱的氧化物不一定是碱性氧化物 ⑦不能跟酸反应的氧化物一定能跟碱反应
A.①②③④ B.⑤⑥⑦ C.②③⑥⑦ D.③⑥
9、在一定的温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原来的温度,下列说法正确的是
A.溶液中溶液中Na+浓度增大,有O2放出 B.溶液中OH-总数不变,有O2放出
C.溶液的pH增大,有O2放出 D.溶液中Na+总数减少,有O2放出
8.下列每组三种溶液,各溶液中均含等物质的量的溶质。将三种溶液充分混合后,可能不产生沉淀的是( )
A、Na2SO3、BaCl2、稀HNO3 B、AlCl3、Ba(OH)2、HNO3、
C、FeCl3、KSCN、HCl D、NaAlO2、NaOH、H2SO4
7.某酸根离子RO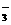 所含电子数比硝酸根离子NO
所含电子数比硝酸根离子NO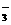 的电子数多10,则下列说法正确的是①R原子的电子层数比N原子的电子层数多1 ②RO
的电子数多10,则下列说法正确的是①R原子的电子层数比N原子的电子层数多1 ②RO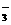 中R元素与NO
中R元素与NO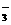 中N元素的化合价相同 ③RO
中N元素的化合价相同 ③RO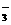 与NO
与NO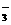 只可能被还原,不可能被氧化 ④R和N不是同周期元素,但是同主族元素( )
只可能被还原,不可能被氧化 ④R和N不是同周期元素,但是同主族元素( )
A.①③④ B.①②④ C.①② D.③④
6.阿伏加德罗常数约为6.02×1023 mol-1,下列叙述中不正确的是( )
A.将162.5g FeCl3转化为氢氧化铁胶体后,氢氧化铁胶体粒子数小于6.02×1023
B.在含196g H2SO4的浓硫酸溶液中加入足量的锌粉使其充分反应,则反应结束时,转移电子数小于4×6.02×1023
C.标准状况下,用NaOH溶液吸收氯气22.4L,反应中转移的电子数目为NA.
D.3.2g铜在硫蒸气中完全燃烧,转移的电子数为0.1NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com