
题目列表(包括答案和解析)
17.(8分)(1)试将下列配制l00mL 0.100mol/L的碳酸钠溶液的操作步骤按先后顺序排列为 (填数字序号)
①将一定质量的碳酸钠置一烧杯内,用少量水将其溶解。
②待溶液冷至室温后,将其完全转移到容量瓶内,摇匀。
③计算所需碳酸钠的质量,并用精密天平称取所需质量的碳酸钠。
④加水至容量瓶内,使凹液面最低点与容量瓶的刻度线相切,盖上塞子摇匀。
⑤检查容量瓶是否渗漏。
现若量取20.00mL该碳酸钠溶液,应选用的仪器是
(2)下列实验操作或对实验事实的叙述正确的是 (填序号)
① 为了提高纯锌与稀硫酸反应的速率,可向稀硫酸中滴入几滴CuSO4溶液
②中和热测定实验时,用铜质搅拌棒代替环形玻璃搅拌棒,所得的中和热的数值会偏低
③使用胶头滴管的任何实验都不允许将滴管插入液面以下
④ 为了获得胆矾晶体,可将CuSO4溶液蒸干、灼烧到质量不再发生变化时为止
⑤ 不慎将苯酚溶液沾到皮肤上,立即用酒精清洗;
⑥ 用石英坩埚高温熔融NaOH和Na2CO3的固体混合物
⑦配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;
⑧用洁净的玻璃棒蘸取浓HNO3,点在pH试纸中部以测定此浓HNO3的pH
⑨用滤纸过滤,可把溶液和胶体分离开来
15.根据下表下列叙述中正确的是:
|
序号 |
氧化剂 |
还原剂 |
其它反应物 |
氧化产物 |
还原产物 |
|
① |
Cl2 |
FeBr2 |
|
|
FeCl3 |
|
② |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
MnSO4 |
|
③ |
KClO3 |
HCl(浓) |
|
Cl2 |
Cl2 |
|
④ |
KMnO4 |
HCl(浓) |
|
Cl2 |
MnCl2 |
A.表中第①组反应的氧化产物一定只有FeCl3(实为Fe3+)
B.氧化性比较: KMnO4>Cl2>Fe3+>Br2>Fe2+
C.还原性比较: H2O2>Mn2+>Cl-
D.④的离子方程式配平后,H+的化学计量数为16
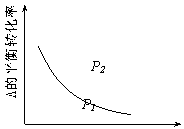

 16某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):
16某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):
|
|||||||||||
 |
|||||||||||
|
|||||||||||
 |
|||||||||||
 |
|||||||||||
 |
|||||||||||
|
|
|
|
|

根据以上规律判断,下列结论正确的是
A.反应Ⅰ:△H>0,P2>P1
B.反应Ⅱ:△H<0,T1>T2
C.反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1
D.反应Ⅳ:△H<0,T2>T1
班级 姓名 学号 成绩
第Ⅱ卷(选择题共86分 )
14、下列各组离子一定能大量共存的是
A、在c(H+)=10-13mol·L-1的溶液中:NH4+、Al3+、SO42-、NO3-
B、在pH=1的溶液中:K+、Fe2+、Cl-、NO3-
C.在c(H+)=10-14mol/L的溶液中可能含:Na+,A102-,CO32-,SO32-
D. 某溶液,加铝粉有氢气放出,则溶液中可能含:K+,Na+,H+,NO3-
13.设NA为阿伏加德罗常数,下列叙述正确的是
A 在1 L 2 mol/L的醋酸钠溶液中含有的醋酸根离子数为
B 1molH2O2与MnO2充分反应转移2NA个电子
C将标准状况下,22.4LH2和4gHe均含有NA个分子
D 50℃1×105pa下,46gNO2与0℃2×105pa下46gN2O4均含有3NA个电子
12.已知HF比CH3COOH易电离。关于物质的量浓度、体积都相同的NaF溶液和CH3COONa溶液,下列说法正确的是
A.CH3COONa溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
B.在相同条件下,两溶液的pH大小为: CH3COONa< NaF
C.NaF溶液中:c(H+)+c(HF)= c(OH-)
D.两溶液相比较,NaF溶液中的离子总数较多
11.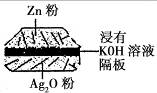 如图:一种微型钮扣电池,其电极材料分别为Ag2O和Zn,电解质溶液是KOH 溶液。负极的反应式:Zn一2e-+2OH-==ZnO+H2O,该电池总反应式为:Zn+Ag2O==ZnO+2Ag。 根据以上提供的资料,判断下列说法正确的是
如图:一种微型钮扣电池,其电极材料分别为Ag2O和Zn,电解质溶液是KOH 溶液。负极的反应式:Zn一2e-+2OH-==ZnO+H2O,该电池总反应式为:Zn+Ag2O==ZnO+2Ag。 根据以上提供的资料,判断下列说法正确的是
A.正极的反应式:Ag2O+2e-+H2O==2Ag+2OH-
B.放电时负极附近溶液的pH不变
C.放电时每消耗6.5g Zn,转移电子0.1mol
D.放电时溶液中阴离子向正极方向移动,阳离子向负极方向移动
10.下列反应的离子方程式正确的是
A.Al投入NaOH溶液:2Al+2OH-+H2O=2AlO2-+3H2↑
B.向硅酸钠溶液中通入过量的CO2: SiO32- + CO2 + H2O = H2SiO3↓+ CO32-
C.在溶液中亚硫酸氢铵与等物质的量的氢氧化钠混合:NH +HSO
+HSO +2OH-==SO
+2OH-==SO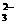 +NH3↑+2H2O
+NH3↑+2H2O
D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全:
Ba2+ + 2OH- + NH4+ +H+ + SO42- = BaSO4↓+ NH3·H2O + H2O
9.有五个系列同族元素的物质,101.3kP时测定它们的沸点(℃)如下表所示:
|
① |
He -268.8 |
(a) -249.5 |
Ar -185.8 |
Kr 151.7 |
|
② |
F2 -187.0 |
Cl2 -33.6 |
(b) 58.7 |
I2 184.0 |
|
③ |
(c) 19.4 |
HCl -84.0 |
HBr -67.0 |
HI -35.3 |
|
④ |
H2O 100.0 |
H2S -60.0 |
(d) -42.0 |
H2Te -1.8 |
|
⑤ |
CH4 -161.0 |
SiH4 -112.0 |
GeH4 -90.0 |
(e) -52.0 |
对应表中内容,下列叙述中正确的是
A.a、 b、c的化学式分别为Ne、Br2、HF
B. 系列②物质均有氧化性;系列③物质对应水溶液均是强酸
C.系列④中各化合物的稳定性顺序为:H20>H2S>H2Se>H2Te
D.上表内物质HF和H2O,由于氢键的影响,其分子特别稳定
8.下列各组物质用一种试剂不能加以鉴别的是
A.NaCl溶液、MgCl2溶液、KNO3溶液、Al2(SO4)3溶液
B.苯、苯酚溶液、己烯和乙醇
C.Na2SO4溶液、Na2SO3溶液、Na2CO3溶液、NaAlO2溶液
D.NaCl溶液、NH4Cl溶液、(NH4)2SO4溶液、Na2SO4溶液
7.下列合成溴化钾的方法中,最合理的是
A.KCl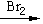 KBr B.Br2
KBr B.Br2 FeBr3
FeBr3 KBr
KBr
C.Br2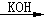 KBr D.KOH
KBr D.KOH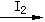 KI
KI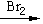 KBr
KBr
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com