
题目列表(包括答案和解析)
6.( )反应热可视为:旧键断裂时吸收的能量和新键形成时释放能量相抵消后的总效应。白磷(P4)和P4O6的分子结构如下图所示。已知:拆开1 molP-P键 吸收198kJ·mol-1、拆开1 mo氧气分子内氧原子间的键,吸收 498kJ·mol-1 ;形成1 mol P-O 键释放360 kJ·mol-1。则P4+3O2 =P4O6的反应热∆H为
 A.+1638 kJ·mol-1 B.-1638 kJ·mol-1
A.+1638 kJ·mol-1 B.-1638 kJ·mol-1
C.-126 kJ·mol-1 D.+126 kJ·mol-1
5.( )一定质量的Na、K分别投入一定量的稀盐酸中,在相同条件下产生氢气的体积随时间变化的曲线如图中a、b所示,则下列说法中正确的是
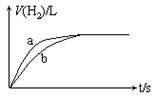 A 投入的Na、K物质的量一定相等
A 投入的Na、K物质的量一定相等
B 曲线a对应的反应使用了催化剂
C 曲线a代表Na的反应,曲线b代表K
D 两反应中盐酸必须是足量的
4.( )4.6gNa与足量的水反应,反应中钠失去的电子数为:
A 0.2 B 0.2 mol C 1.204 × 1023 D 0.1 mol
3.( )在14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4中,下列说法正确的是
A 产物中的SO42-离子只有-部分是氧化产物
B 1mol CuSO4能氧化硫的物质的量是0.5mol
C Cu2S既是氧化产物又是还原产物
D CuSO4是氧化剂,FeS2是还原剂
2.( )下列各组离子中,一定能大量共存的是
A.加入铝粉有氢气产生的溶液中:Na+、SO42-、Cl-、Mg2+、
B.滴加石蕊试液显红色的溶液中:Fe3+、NH4+、Cl-、SCN-
C.在0.1mol/L的NaHSO4溶液中:NH4+、Na+、Al3+、Cu2+、NO3-
D.在0.1mol/L的NaHCO3溶液中K+、Al3+、Fe3+、NO3-
1.( )韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成了“暖冰”。下列关于“暖冰”的说法不正确的是
A.“暖冰”也是水分子间通过氢键结合而成的固体
B.水凝固形成20℃时的“暖冰”所发生的变化是化学变化
C.形成20℃时的“暖冰”的变化是物理变化
D.在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰”
28、(14分)
(1)E__ ____,F_ ___,G___ ___。
(2)①__________ __________,
④___ __________________。
(3) _____ __________; ___________ ____。
27、(8分)(1)为 、 。
(2)___________。________________________。
26、(12分)
(1)_____________________。(2)___________________________ ______。
(3)_____________________ ___________。
(4):__________ _____。________极,其原因是:___________________________
_ _
25、(8分):
(1)固体A属于 晶体,它的电子式为_________________;
(2)原因___ __________ __ __。
(3)_________________ __________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com